
심방세동(atrial fibrillation, AF)은 전 세계적으로 약 5,900만 명에 영향을 미치는 가장 흔한 지속성 심장 부정맥입니다[1]. 이 질환은 뇌졸중 위험을 최대 5배까지 높이는 것으로 알려져 있으며[2], 조기에 발견하고 적절히 대처하는 것이 장기적 예후에 결정적인 영향을 미칩니다.
심방세동은 심장의 위쪽 두 방, 즉 심방(atrium)이 정상적인 전기 신호 없이 분당 300~600회에 달하는 불규칙한 세동(fibrillation)을 일으키는 상태입니다. 정상적인 심박수가 분당 60~100회 수준인 것과 비교하면, 심방이 사실상 '떨리고' 있는 상태에 가깝습니다. 심방의 수축 기능이 사라지면서 혈액이 효과적으로 심실로 전달되지 못하고, 심박수도 불규칙하게 됩니다.
2020년 유럽심장학회(European Society of Cardiology, ESC) 가이드라인에서는 심방세동을 발작성(paroxysmal), 지속성(persistent), 영구성(permanent)의 세 가지 패턴으로 분류합니다[3]. 발작성 심방세동은 7일 이내에 자연 종료되는 유형이며, 지속성은 7일 이상 지속되어 약물 또는 전기적 처치가 필요한 경우를 말합니다. 영구성은 심율동 전환(cardioversion)이 더 이상 시도되지 않는 만성 상태입니다.
증상은 개인차가 크지만 대표적으로 다음과 같은 증상이 나타납니다. 가슴이 두근거리거나 빠르게 뛰는 느낌(심계항진, palpitation), 숨이 차는 느낌(호흡곤란), 가슴 불편감, 어지러움, 피로감이 흔히 보고됩니다. 운동 시 또는 안정 시 모두 발생할 수 있으며, 일부에서는 실신으로 이어지기도 합니다.
주목할 점은 심방세동 환자의 약 3분의 1이 아무런 증상을 경험하지 못한다는 것입니다[4]. 이를 무증상 심방세동(silent atrial fibrillation)이라고 하며, 이 경우 뇌졸중이 첫 번째 임상 징후로 나타나는 경우도 드물지 않습니다. 65세 이후 발작성 심방세동의 경우, 전체 삽화의 50~70%가 환자가 자각하지 못하는 상태에서 발생한다는 연구 결과도 있습니다[4].
50대 후반 남성 A씨는 평소 가끔 느끼던 두근거림을 과로 탓으로만 여겨 왔습니다. 정기 건강검진에서 심전도(electrocardiogram, ECG) 검사를 받은 결과 발작성 심방세동으로 진단되었고, 당시 이미 CHA2DS2-VASc 점수가 2점으로 항응고치료 적응증에 해당되었습니다. A씨처럼 자각 증상이 경미해도 부정맥 자체는 상당히 진행되어 있을 수 있습니다.
두근거림이 하루에 수차례 반복되거나, 수 분 이상 지속되는 불규칙한 심박이 느껴지거나, 특별한 이유 없이 숨이 차고 어지럽다면 심방세동을 의심하고 심전도 검사를 받는 것이 적절합니다. 특히 60세 이상이거나 고혈압, 당뇨, 심장질환의 기왕력이 있는 경우 증상 없이도 정기적인 심전도 검사가 권고됩니다[3].
심방세동이 위험한 가장 큰 이유는 뇌졸중 발생 위험을 크게 높이기 때문입니다. 심방이 정상적으로 수축하지 못하면 혈액이 심방 내에 고이고, 특히 좌심방이(left atrial appendage, LAA)에 혈전(thrombus)이 형성될 가능성이 높아집니다. 이 혈전이 떨어져 나와 뇌 혈관을 막으면 뇌졸중이 발생합니다[2]. 심방세동 관련 뇌졸중은 일반 뇌졸중에 비해 범위가 넓고 예후가 더 불량한 경향이 있습니다.
뇌졸중 위험을 수치화하기 위해 임상에서 널리 사용되는 도구가 CHA2DS2-VASc 점수입니다. 이 점수는 다음 항목으로 구성됩니다. 심부전(congestive heart failure) 1점, 고혈압(hypertension) 1점, 나이 75세 이상 2점, 당뇨(diabetes mellitus) 1점, 뇌졸중 또는 일과성 허혈 발작(transient ischemic attack, TIA) 과거력 2점, 혈관 질환(vascular disease) 1점, 나이 65~74세 1점, 여성(sex category) 1점으로 최대 9점입니다[5].
2023년 미국심장학회(American College of Cardiology, ACC)와 미국심장협회(American Heart Association, AHA)의 공동 가이드라인에 따르면 CHA2DS2-VASc 점수 0점인 경우 항혈전 치료 없이 경과 관찰이 가능합니다. 1점인 경우 구체적 임상 상황에 따라 판단이 필요하며, 2점 이상이면 경구 항응고제(oral anticoagulant) 투여가 권고됩니다[5]. 단순히 점수가 높을수록 뇌졸중 발생률도 비례하여 증가하는 패턴이 확인됩니다.
심방세동의 패턴도 뇌졸중 위험에 영향을 미칩니다. 대규모 연구에서 비발작성(non-paroxysmal) 심방세동은 발작성보다 뇌졸중 위험이 더 높으며, 심방세동의 지속 시간(burden)이 길어질수록 위험이 증가합니다[6]. 5분 이상의 심방세동 부담(AF burden)은 뇌졸중 위험을 2.49배(95% 신뢰구간: 1.79~3.47) 높이는 것으로 보고됩니다[6].
60대 초반 여성 B씨는 고혈압과 당뇨를 함께 앓고 있었으며, 어느 날 갑자기 발생한 심한 어지럼증과 언어 장애로 응급실을 방문했습니다. 뇌졸중 진단을 받은 후 심전도 검사에서 비로소 심방세동이 확인되었습니다. B씨의 CHA2DS2-VASc 점수는 고혈압 1점, 당뇨 1점, 65세 미만 여성 1점으로 총 3점에 해당했으며, 사전에 항응고치료를 받았더라면 뇌졸중 예방 가능성이 있었습니다.
나이, 고혈압, 당뇨, 심부전, 이전 뇌졸중 등 복수의 위험 인자를 가진 경우 전문의와의 상담을 통해 CHA2DS2-VASc 점수를 직접 확인하고 항응고치료 필요성을 논의하는 것이 중요합니다. 점수가 낮더라도 증상이 반복되거나 심전도 이상이 발견되면 추적 관찰이 필요합니다.
심방세동의 일차 진단 도구는 12유도 심전도(12-lead ECG)입니다. 심전도에서 P파가 소실되고 불규칙한 RR 간격이 관찰되면 심방세동으로 진단합니다. 발작성 심방세동은 검사 시점에 삽화가 없으면 정상 심전도로 나타날 수 있어 24~48시간 홀터 모니터링(Holter monitoring) 또는 장기 심장 모니터링이 필요할 수 있습니다[3].
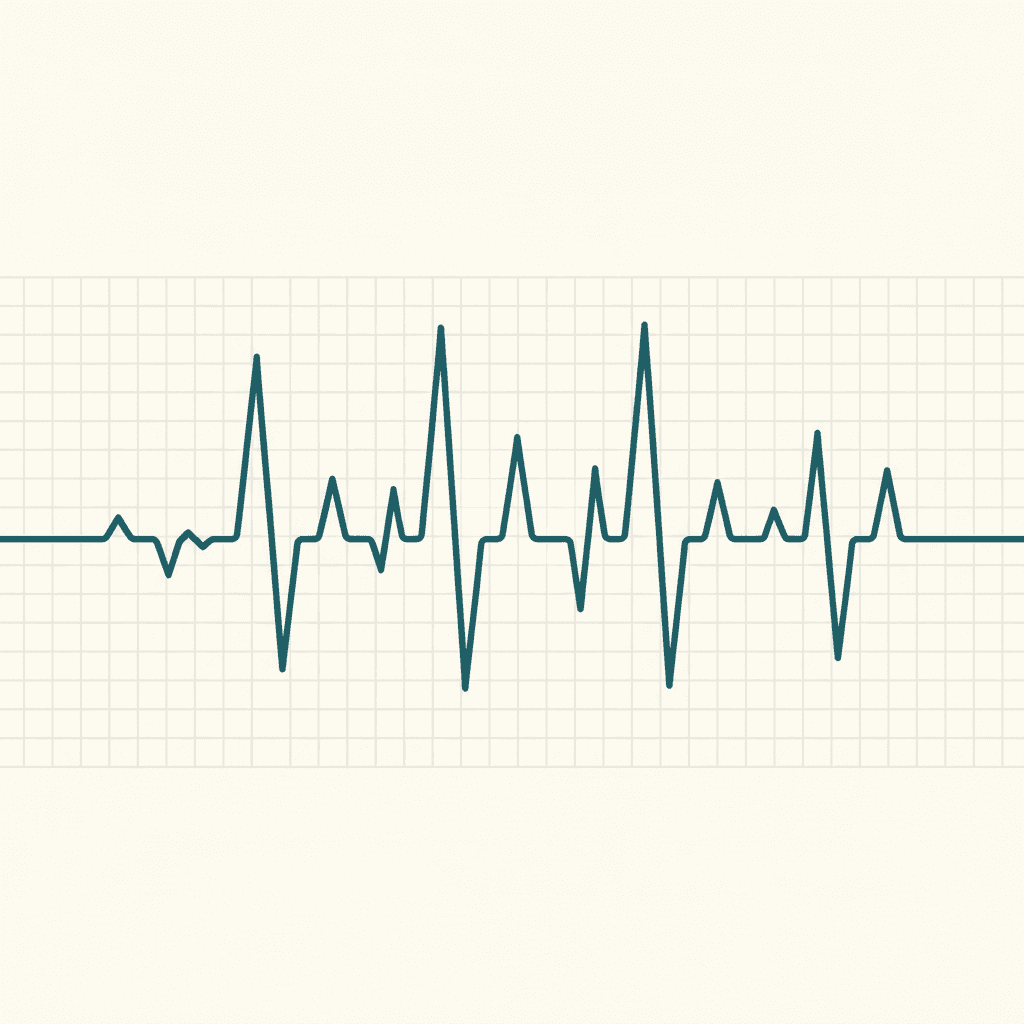
무증상 심방세동은 일반 심전도 검사로 놓치기 쉽습니다. 최근에는 스마트워치나 패치형 심전도 기기를 이용한 장기간 원격 모니터링이 주목받고 있습니다. 연구에 따르면 14일간의 지속 심장 모니터링(prolonged cardiac monitoring)은 심방세동 탐지율을 표준 심전도에 비해 유의미하게 높이며, 탐지된 심방세동의 뇌졸중 재발 위험도 평가에 중요합니다[7].
항응고치료는 심방세동 관련 뇌졸중 예방의 핵심입니다. 현재 임상에서는 직접 경구 항응고제(direct oral anticoagulant, DOAC), 즉 다비가트란(dabigatran), 리바록사반(rivaroxaban), 아픽사반(apixaban), 에독사반(edoxaban)이 와파린(warfarin)을 대체하는 1차 치료제로 권고됩니다[5]. 대규모 무작위 대조 시험의 개인 데이터 메타분석에 따르면, 표준 용량의 DOAC는 와파린 대비 뇌졸중 또는 전신 색전증 발생률이 더 낮으며(3.01% 대 3.69%), 두개내 출혈 위험도 유의하게 낮습니다[8].
심방세동의 치료는 항응고치료 외에도 심박수 조절(rate control)과 심율동 전환(rhythm control)을 포함합니다. 심박수 조절은 베타차단제(beta-blocker), 칼슘 채널 차단제 등을 이용해 심박수를 분당 80~110회 이내로 유지하는 방법입니다. 심율동 전환은 약물 또는 직류 전기 충격을 통해 정상 동율동(sinus rhythm)을 회복시키는 방법으로, 증상 조절과 심기능 유지에 기여합니다.
카테터 절제술(catheter ablation)은 폐정맥(pulmonary vein) 주변의 이상 전기 신호 발생 부위를 차단하는 시술로, 발작성 심방세동에서 특히 효과적인 것으로 알려져 있습니다. 약물 치료로 증상이 충분히 조절되지 않거나 심기능 저하가 동반된 경우 고려됩니다[5].
심방세동 또는 이와 유사한 증상이 의심될 때 진료를 받아야 하는 상황을 명확히 이해하는 것이 중요합니다. 갑작스럽고 빠른 심계항진이 수 분 이상 지속되거나 반복될 때, 가슴 통증이나 호흡곤란이 동반될 때, 어지러움이나 기절이 발생할 때는 가급적 빠른 시일 내에 심전도 검사가 필요합니다.
특히 다음과 같은 상황은 즉각적인 응급 처치가 필요합니다. 갑자기 한쪽 얼굴이나 팔다리에 힘이 없어지는 경우, 말이 갑자기 어눌해지거나 이해가 안 되는 경우, 갑작스러운 심한 두통이 발생하는 경우, 시야가 갑자기 흐려지거나 한쪽이 안 보이는 경우가 해당됩니다. 이는 뇌졸중의 전형적인 급성 증상으로, 즉시 응급실을 방문해야 합니다. 골든 타임 이내의 처치 여부가 예후를 크게 결정합니다.
이미 심방세동으로 진단받은 경우라면 처방된 항응고제를 의사의 지도 없이 임의로 중단하지 않아야 합니다. 항응고제를 갑자기 중단하면 혈전 형성 위험이 급격히 높아질 수 있기 때문입니다. 음주는 심방세동 삽화를 유발하거나 악화시킬 수 있어 절제가 필요하며, 적정 체중 유지, 고혈압과 당뇨의 적극적 관리, 규칙적인 유산소 운동이 전반적인 심혈관 위험을 낮추는 데 도움이 됩니다.
정기적인 추적 검사도 중요합니다. 심방세동 환자는 심전도 검사뿐만 아니라 심초음파(echocardiography)를 통한 심기능 평가, 신장 기능 검사(항응고제 용량 조정에 필요), 갑상선 기능 검사 등을 정기적으로 시행합니다. 2023년 ACC/AHA 가이드라인은 심방세동 환자의 통합적 관리를 위해 뇌졸중 예방, 증상 조절, 심혈관 동반 질환 관리의 세 축을 균형 있게 다룰 것을 권고하고 있습니다[5].
Q1. 심방세동이 있으면 반드시 증상이 나타나나요?
그렇지 않습니다. 심방세동 환자의 약 3분의 1은 증상을 경험하지 못하며, 발작성 심방세동의 경우 삽화의 절반 이상이 자각 없이 지나가는 것으로 보고됩니다[4]. 증상이 없다고 해서 뇌졸중 위험이 낮은 것은 아니므로 위험 인자가 있는 경우 정기적인 심전도 검사가 중요합니다.
Q2. CHA2DS2-VASc 점수가 1점이면 항응고제를 꼭 복용해야 하나요?
1점의 경우 임상 지침에 따라 담당 의사와 개별적으로 논의하는 것이 적절합니다. 성별에 따른 1점(여성)은 독립적인 위험 인자로 인정되지 않는 경우도 있어, 실제 위험 평가는 점수 외에도 추가 임상 정보를 함께 고려합니다[5]. 2점 이상이면 경구 항응고제 투여가 명확히 권고됩니다.
Q3. DOAC와 와파린 중 어느 것이 더 좋은가요?
대규모 메타분석 결과에 따르면, DOAC는 와파린 대비 뇌졸중 또는 전신 색전증 예방 효과가 유사하거나 우월하며 두개내 출혈 위험은 더 낮습니다[8]. 신장 기능, 약물 상호작용, 환자의 순응도 등 개인적 요인에 따라 선택이 달라질 수 있어 의사와 상담 후 결정합니다.
Q4. 심방세동은 완치가 되나요?
발작성 심방세동의 경우 카테터 절제술 이후 수년간 동율동을 유지하는 경우가 있습니다. 그러나 심방세동은 재발 가능성이 있으며, 특히 오래 지속된 경우나 기저 심장 질환이 있는 경우 완전한 완치보다는 장기적인 관리가 필요한 만성 질환으로 이해하는 것이 적절합니다[3].
Q5. 심방세동인데 운동을 해도 괜찮은가요?
규칙적인 중강도 유산소 운동은 심방세동 환자의 심혈관 건강과 증상 조절에 긍정적인 영향을 미친다고 알려져 있습니다. 다만 운동 강도와 종류는 개인의 심기능 상태, 항응고치료 여부, 동반 질환에 따라 달라지므로 운동 프로그램 시작 전 담당 의료진과 먼저 확인하는 것이 필요합니다.
[1] Lippi G, et al. Global epidemiology of atrial fibrillation: An increasing epidemic and public health challenge. Int J Stroke. 2021;16(2):217-221. PMID: 31955707.
[2] Kamel H, Okin PM, Elkind MS, Iadecola C. Atrial fibrillation and mechanisms of stroke. Stroke. 2016;47(3):895-900. https://doi.org/10.1161/strokeaha.115.012004
[3] Hindricks G, et al. 2020 ESC Guidelines for the diagnosis and management of atrial fibrillation. Eur Heart J. 2021;42(5):373-498. PMID: 32860505.
[4] Siontis KC, et al. Silent atrial fibrillation: epidemiology, diagnosis, and clinical impact. Clin Cardiol. 2017;40(6):413-418. PMID: 28273368.
[5] Joglar JA, et al. 2023 ACC/AHA/ACCP/HRS Guideline for the Diagnosis and Management of Atrial Fibrillation. Circulation. 2024;149(1):e1-e156. https://doi.org/10.1161/CIR.0000000000001193
[6] Ganesan AN, et al. Atrial fibrillation burden and the risk of stroke: A systematic review and dose-response meta-analysis. J Am Heart Assoc. 2022;11(4):e023482. PMID: 35127908.
[7] Bernstein RA, et al. Differences in stroke recurrence risk between atrial fibrillation detected on ECG and 14-day cardiac monitoring. Neurology. 2023;101(3):e308-e315. PMID: 37377007.
[8] Grymonprez M, et al. Direct oral anticoagulants versus warfarin in patients with atrial fibrillation: patient-level network meta-analyses of randomized clinical trials with interaction testing by age and sex. Circulation. 2022;145(4):242-255. PMID: 34985309.
본 콘텐츠는 학술 논문과 공개된 연구 자료를 바탕으로 작성된 정보성 글이며, 의학적 진단이나 치료를 대체하지 않습니다. 건강 관련 결정은 반드시 담당 의료진과 상담하시기 바랍니다.