
전분을 섭취하는 순간부터 신체는 즉각적인 분해 과정에 돌입합니다. 그 과정을 주도하는 첫 번째 핵심 효소가 바로 아밀라아제(Amylase)입니다. 이 글은 아밀라아제의 생화학적 기전부터 최신 임상 연구 결과까지, 근거 중심으로 정리합니다.
스폰서 콘텐츠 안내: 이 글은 닥터블릿의 제품 정보를 바탕으로 작성된 분석 콘텐츠입니다. 편집팀은 독립적 검증을 거쳐 객관성을 유지합니다.
알파-아밀라아제(Alpha-amylase)는 전분의 알파-1,4-글리코시드(alpha-1,4-glycosidic) 결합을 무작위로 절단하는 내부 가수분해 효소입니다. 이 효소는 타액선과 췌장 두 부위에서 분비되며, 식이 탄수화물 소화의 초기 단계를 담당합니다. 효소 없이는 복합 탄수화물이 포도당 단위로 전환되는 과정이 현저하게 지연되고, 소장에서의 흡수 효율도 낮아집니다. 타액 아밀라아제와 췌장 아밀라아제는 동일한 반응을 서로 다른 환경에서 수행하는 상호 보완적 구조를 이룹니다.
타액 아밀라아제(Salivary Amylase, SAA)는 구강에서 분비되는 즉시 전분 분해를 시작합니다. 연구에 따르면 빵 전분의 최대 80%가 위 내 소화 30분 동안 타액 아밀라아제에 의해 분해될 수 있습니다. 이는 위산 환경에서도 아밀라아제 활성이 일정 수준 유지됨을 보여주는 수치입니다. 즉, 구강부터 시작된 아밀라아제 반응은 식괴(食塊)가 위를 통과하는 동안에도 지속적으로 진행됩니다. 췌장 아밀라아제는 소장 상부에서 이 과정을 이어받아 전분 분해를 완결하며, 두 효소의 연속 작용으로 맥아당과 올리고당이 생성됩니다.
아밀라아제 활성에는 개인 간 상당한 차이가 존재합니다. 그 핵심 원인은 AMY1 유전자의 복제 수 변이(Copy Number Variation, CNV)입니다. AMY1 복제 수가 많은 개인일수록 타액 아밀라아제 분비량이 증가하고, 이에 따라 식후 혈당 반응의 크기도 달라집니다 [5,6]. 이러한 유전적 다형성은 동일한 식사를 섭취하더라도 탄수화물 대사 결과가 사람마다 다른 이유를 분자 수준에서 설명합니다. 즉 아밀라아제 활성은 단순한 소화 속도의 문제가 아니라, 혈당 조절과 대사 효율에도 영향을 미치는 생리적 변수입니다.
아밀라아제가 소화관 구조 자체에 미치는 영향도 중요한 연구 주제로 부상하고 있습니다. Zaworski 등(2024)의 돼지 모델 연구(n=22)에서 미생물 유래 아밀라아제를 보충하면 소장 융모(villus) 길이와 음와(crypt) 깊이가 췌장 소화효소제(pancrelipase)와 비교할 만한 수준으로 회복되었습니다 [4]. 융모 구조는 영양소 흡수 면적을 결정하고, 음와는 상피세포 재생의 기원이 되는 곳입니다. 이 두 지표가 아밀라아제 보충을 통해 유지된다는 것은, 효소 공급이 소화 촉진을 넘어 장 점막 항상성 유지에도 기여함을 시사합니다. 다만 이 연구는 동물 모델에 기반하므로, 인체에서의 동일한 효과를 직접 확인하려면 별도의 임상 연구가 필요합니다.
아밀라아제 활성은 내인적 요인 외에도 외인적 요인에 의해 조절됩니다. 흰강낭콩 추출물에 포함된 파세올라민(phaseolamin)은 아밀라아제 억제제로 작용하여 효소 활성을 직접적으로 낮춥니다. 양성자 펌프 억제제(PPI) 계열 약물은 위산을 억제함으로써 위 내 pH 환경을 변화시키고, 이는 타액 아밀라아제가 위에서 활성을 유지하는 시간에 영향을 줄 수 있습니다. 따라서 소화 효소 보충을 고려할 때는 현재 복용 중인 약물과의 상호작용을 함께 검토하는 것이 임상적으로 중요합니다. 효소 활성에 영향을 미치는 이러한 요인들은 보충제 선택과 복용 방식을 결정할 때 실질적인 기준이 됩니다.
아밀라아제의 최적 작용 조건은 온도와 pH에 의해 결정됩니다. 인체 타액 아밀라아제는 pH 6.7~7.0, 체온(37°C) 부근에서 최고 활성을 나타냅니다. 위 내 pH가 2.0 이하로 낮아지면 활성이 크게 저하되지만, 식괴에 의해 완충된 위 내부에서는 pH가 일시적으로 상승하여 효소 활성이 유지되는 시간이 연장됩니다. 이러한 pH 동태는 아밀라아제가 구강과 위를 거쳐 소장으로 이행하는 동안 얼마나 효율적으로 작용하는지를 결정하는 핵심 변수입니다. 효소의 열 안정성과 pH 내성은 외인성 효소 보충제 개발에서 중요한 설계 기준으로 활용됩니다.

소화 효소 보충이 기능성 소화불량(Functional Dyspepsia)에 미치는 효과를 평가한 고품질 임상 연구가 최근 여러 편 발표되었습니다. 이 연구들은 소화 효소 복합 보충제의 유용성을 검토하는 데 있어 중요한 근거 기반을 형성합니다. 각 연구의 설계와 결과를 구분하여 살펴보면, 보충제의 작용 범위를 보다 정확하게 파악할 수 있습니다.
Ullah 등(2023)은 기능성 소화불량 환자 120명을 대상으로 균류 발효(Fungal Fermentation) 유래 다중 효소 혼합물 200 mg을 1일 2캡슐씩 2개월간 투여하는 이중맹검 위약 대조 무작위 임상시험(RCT)을 수행하였습니다 [2]. 결과적으로 기능성 소화불량 증상 지수(NDI-SF), 통증 시각적 아날로그 척도(VAS), 수면의 질 평가 척도(PSQI) 모두에서 위약군 대비 유의미한 개선이 나타났습니다. 이 연구에서 이상 반응은 시험 기간 동안 보고되지 않았으며, 2개월간의 복용이 안전하게 진행되었습니다. 이 결과는 균류 발효 유래 다중 효소가 소화 기능 개선 외에도 수면의 질과 같은 전반적인 삶의 질 지표에까지 영향을 미칠 수 있음을 보여줍니다.
아밀라아제와 프로바이오틱스를 결합한 복합 보충제 연구도 주목할 만한 결과를 보여줍니다. La Monica 등(2023)의 RCT(n=52, 6주)에서 프로바이오틱스-아밀라아제 복합 보충군은 위장 증상 평가 척도(Gastrointestinal Symptom Rating Scale, GSRS) 점수를 약 60% 감소시킨 반면, 위약군은 약 25% 감소에 그쳤습니다 [1]. 복부 팽만감 항목에서는 보충군 49% 감소 대 위약군 25% 감소의 차이가 관찰되었으며, 복부 불편감은 각각 59% 대 32%의 차이를 보였습니다. 이 연구의 효과는 아밀라아제 단독 성분이 아닌 프로바이오틱스와의 병용 효과를 반영하므로, 아밀라아제 단독 효과로 해석하는 것은 적절하지 않습니다. 그럼에도 불구하고 아밀라아제를 핵심 성분으로 포함한 복합 보충제가 위장 증상에 대해 의미 있는 개선 효과를 보였다는 점에서 중요한 근거가 됩니다.
같은 연구 그룹이 발표한 후속 연구(Ghannoum et al., 2024)는 장내 미생물 구성의 변화를 분석하였습니다 [3]. 6주간의 보충 후 유익균인 Saccharomyces cerevisiae의 비율이 기저치 약 20%에서 약 60%로 약 200배 증가하였으며, 유해 미생물의 비율은 감소하는 방향으로 변화하였습니다. 또한 9종의 미생물이 32가지 위장 기능 지표와 연관성을 갖는 것으로 확인되었습니다. 다만 이 연구는 산업계 공동 자금 지원이 포함되어 있어 결과 해석에 신중함이 필요합니다. 그럼에도 이 데이터는 아밀라아제 기반 보충이 효소 활성 제공을 넘어 장내 미생물 생태계의 변화와 연관될 수 있음을 시사하는 탐색적 근거를 제공합니다.
타액 아밀라아제 활성과 혈당 반응의 관계를 직접 검증한 연구도 있습니다. Mandel과 Breslin(2012)의 교차 설계 RCT(n=14)에서는 타액 아밀라아제 고활성 개인이 전분 섭취 후 45분, 60분, 75분 시점에서 저활성 개인 대비 식후 혈당이 유의하게 낮았습니다(p<0.05) [7]. 최고 혈당값(peak glucose)과 혈당 곡선하면적(AUC, Area Under the Curve) 모두 고활성 군에서 낮게 나타났습니다. 이는 아밀라아제 활성 수준이 단순히 소화 속도를 결정하는 것이 아니라, 실질적인 탄수화물 대사 효율과 직접 연관됨을 보여주는 임상 근거입니다. 표본 크기가 작고 2012년 발표된 연구라는 한계가 있으나, 이후 리뷰 논문들에서도 이 결과는 일관되게 인용되고 있습니다.
최신 리뷰 연구들은 SAA 활성의 대사적 함의를 체계적으로 정리하고 있습니다. Erta 등(2026)은 SAA 활성이 식후 혈당 반응, 인슐린 분비, 비만 위험과 연관됨을 논하였습니다 [5]. 동일 저자의 2025년 리뷰는 AMY1 CNV가 개인별 SAA 변동성의 주요 결정 인자임을 분석 도구와 임상적 관점을 종합하여 확인하였습니다 [6]. 이들 리뷰 논문들은 관찰 연구와 기존 RCT를 종합한 것으로, 인과 관계가 아닌 연관성 수준의 근거를 제공합니다. 그럼에도 아밀라아제 연구가 단순 소화 기능을 넘어 대사 의학의 영역으로 확장되고 있음을 보여주는 최신 동향으로서 중요한 의의를 지닙니다.
현재까지의 임상 연구들을 종합하면, 소화 효소 보충의 효과는 대상 집단과 효소 구성에 따라 다르게 나타납니다. 기능성 소화불량 환자 집단에서는 증상 지수와 삶의 질 지표 모두에서 유의미한 개선이 확인되었습니다 [2]. 프로바이오틱스와의 병용에서는 장내 미생물 구성 변화라는 추가적인 효과가 관찰되었으며 [3], 이는 단순 효소 보충과는 다른 작용 경로를 시사합니다. 향후 연구에서는 대규모 표본, 장기 추적, 다양한 연령대와 건강 상태를 포함하는 설계가 필요하며, 현재 근거는 이러한 제한 속에서 해석되어야 합니다.
닥터블릿(Dr.Blet)은 균류 발효 공정 기반의 소화 효소 복합 성분을 핵심으로 구성된 제품 라인을 운영합니다. 균류 발효 유래 효소의 가장 중요한 특성은 동물 췌장 유래 효소 대비 넓은 pH 범위에서 안정적으로 활성을 유지한다는 점입니다. 동물 유래 효소는 주로 소장의 중성 내지 약알칼리 환경에서 최적 활성을 발휘하지만, 균류 유래 효소는 위산 환경(pH 3~5)에서도 어느 정도 활성을 유지합니다. 이 특성은 효소가 소화관 전반에서 보다 일관된 역할을 수행할 수 있는 조건을 형성하는 것으로 이해됩니다.
Ullah 등(2023)의 임상 연구 [2]는 균류 발효 다중 효소 혼합물을 실험 성분으로 사용하였습니다. 해당 연구 성분은 아밀라아제를 포함한 다중 효소 복합 구성이며, 닥터블릿의 소화 효소 접근 방식과 성분 구성 방향에서 공통점이 있습니다. 단, 제품별 성분 함량, 효소 활성 단위, 배합 비율은 제품마다 상이할 수 있으며, 본 연구 결과가 닥터블릿 제품에 직접 적용됨을 의미하지는 않습니다. 편집팀은 공개된 제품 성분 정보와 관련 연구 데이터를 독립적으로 검토하여 이 글을 작성하였습니다.
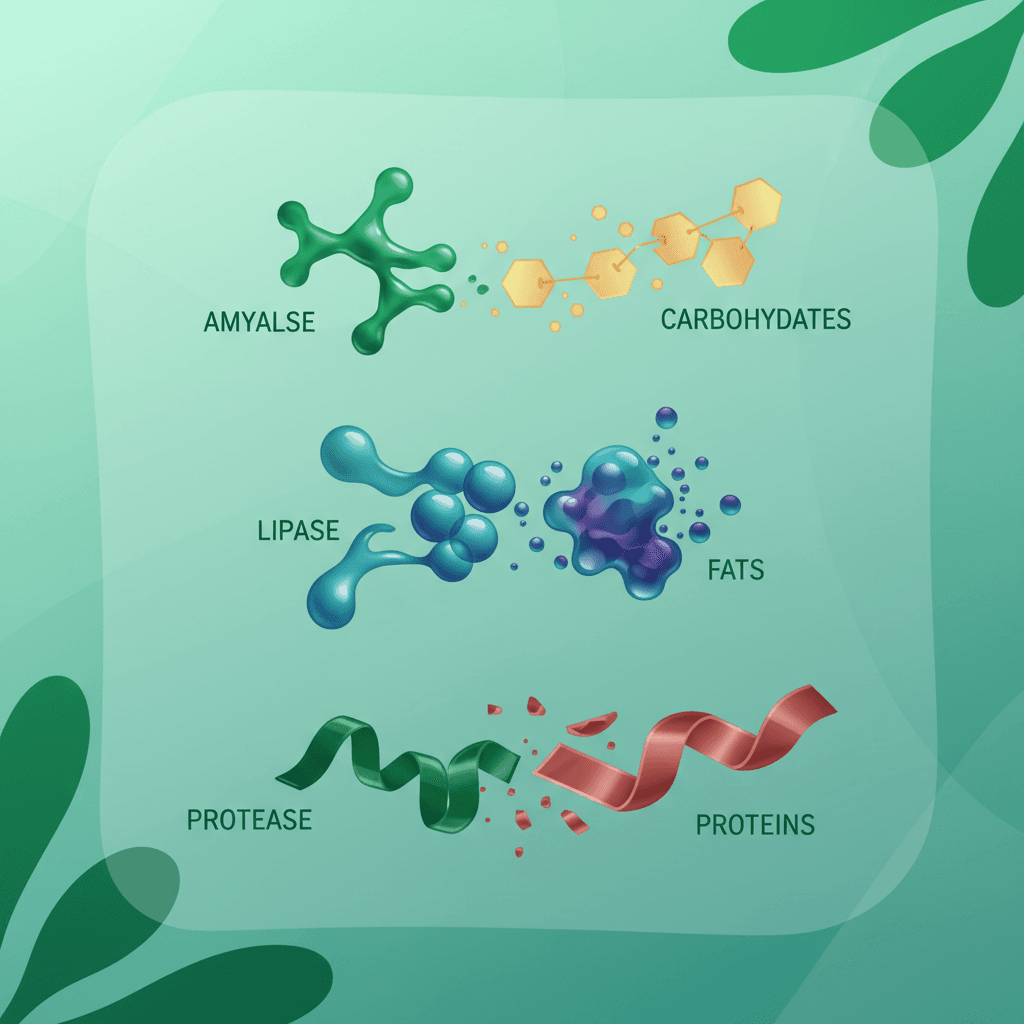
닥터블릿의 복합 효소 설계는 아밀라아제 단독 보충을 넘어서는 구조를 취합니다. 지방 분해 효소인 리파아제(Lipase)와 단백질 분해 효소인 프로테아제(Protease)를 아밀라아제와 함께 배합하여, 탄수화물, 지방, 단백질 세 가지 대량 영양소 전반의 소화를 동시에 지원합니다. 단일 효소 보충은 특정 영양소의 소화만을 목표로 하며 나머지 영양소에는 영향을 주지 않습니다. 반면 다중 효소 복합 설계는 혼합 식사에서 발생하는 다양한 소화 부담을 동시에 처리할 수 있다는 기능적 장점이 있습니다. 이러한 접근은 특히 다양한 식품을 한 끼에 섭취하는 현대 식단 패턴에서 실질적인 의의를 가질 수 있습니다.
La Monica 등(2023) [1]과 Ghannoum 등(2024) [3]의 연구는 아밀라아제 기반 복합 보충이 장내 미생물 구성에 미치는 영향을 실증하였습니다. 닥터블릿 제품은 프로바이오틱스와 소화 효소를 병용하는 설계를 채택하고 있으며, 이는 효소-미생물 상호작용을 통한 장 환경의 종합적 지원이라는 근거 기반 방향과 일치합니다. 프로바이오틱스와 아밀라아제의 병용이 장내 미생물 다양성과 유익균 비율 개선에 기여하는 과정은 아직 완전히 규명되지 않았습니다. 현재로서는 효소에 의한 기질 변화가 특정 미생물의 증식에 유리한 환경을 조성한다는 가설이 제시되고 있으며, 이를 검증하는 추가 연구가 진행 중입니다.
안전성과 복용 시 주의 사항은 소화 효소 보충제 선택에서 빠질 수 없는 고려 항목입니다. 현재까지 발표된 소화 효소 관련 RCT에서는 이상 반응이 보고되지 않았으나 [1,2], 이는 모든 개인에게 동일한 안전성을 보장하지는 않습니다. 균류 유래 성분에 알레르기가 있거나, 특정 성분에 과민 반응 이력이 있는 경우에는 복용 전 반드시 의료진과 상담하는 것이 필요합니다. 아밀라아제 억제제(예: 흰강낭콩 추출물)나 PPI 계열 약물을 동시에 복용 중인 경우, 효소 활성에 영향이 발생할 수 있으므로 담당 의사나 약사와의 확인이 권고됩니다. 소화기 관련 증상이 2주 이상 지속되거나 악화되는 경우에는 보충제 복용보다 전문의를 통한 원인 확인이 우선적으로 필요합니다.
Q1. 아밀라아제는 인체 어디에서 분비되나요?
아밀라아제는 타액선과 췌장 두 부위에서 분비됩니다. 타액 아밀라아제는 구강에서 즉시 전분 분해를 시작하며, 식괴가 위를 통과하는 동안에도 일정 수준의 활성을 유지합니다. 췌장 아밀라아제는 소장 상부에서 분비되어 분해 과정을 완결하며, 두 효소의 연속 작용으로 복합 탄수화물이 흡수 가능한 단당류로 전환됩니다.
Q2. AMY1 복제 수 변이가 탄수화물 소화에 어떤 영향을 미치나요?
AMY1 복제 수는 타액 아밀라아제 분비량을 결정하는 주요 유전적 인자입니다. 복제 수가 많은 개인일수록 타액 아밀라아제 활성이 높고, 전분 섭취 후 식후 혈당 상승 폭이 낮은 경향이 있습니다 [7]. 이 유전적 차이는 동일한 탄수화물을 섭취하더라도 혈당 반응이 사람마다 다른 이유를 분자 수준에서 설명하는 근거입니다.
Q3. 소화 효소 보충은 어떤 대상에서 임상 근거가 있나요?
현재까지 발표된 RCT는 주로 기능성 소화불량 증상이 있는 성인을 대상으로 합니다 [2]. 건강한 일반 성인에 대한 대규모 장기 임상 데이터는 아직 제한적입니다. 증상이 없는 경우의 예방적 복용에 대해서는 추가적인 임상 연구가 필요한 상황입니다.
Q4. 균류 발효 유래 효소는 동물 유래 효소와 어떻게 다른가요?
균류 발효 유래 효소의 가장 큰 특징은 넓은 pH 범위에서 활성을 유지하는 것입니다. 동물 췌장 유래 효소는 주로 소장의 중성에 가까운 환경에서 최적 활성을 나타내는 반면, 균류 유래 효소는 위산 환경에서도 일부 활성을 유지합니다. 이 차이로 인해 균류 유래 효소는 소화관 전반에 걸쳐 보다 지속적인 분해 작용을 기대할 수 있다는 이론적 근거가 있습니다.
Q5. 소화 효소 보충제 복용 시 특별히 주의할 사항이 있나요?
균류 또는 특정 식품에 알레르기가 있는 경우, 복용 전 의료진 상담이 반드시 필요합니다. 아밀라아제 억제제(흰강낭콩 추출물 등)나 PPI 계열 약물을 병용하는 경우 효소 활성이 저하될 수 있으므로 주의가 필요합니다. 소화기 증상이 2주 이상 지속된다면 원인 파악을 위한 전문의 진료를 먼저 받는 것이 바람직합니다.
[1] La Monica et al. "A probiotic amylase blend reduces gastrointestinal symptoms in a randomised clinical study." Beneficial Microbes, 2023. DOI: 10.1163/18762891-20230043. PMID: 38350481.
[2] Ullah et al. "Efficacy of digestive enzyme supplementation in functional dyspepsia: A monocentric, randomized, double-blind, placebo-controlled, clinical trial." Biomedicine & Pharmacotherapy, 2023. DOI: 10.1016/j.biopha.2023.115858. PMID: 37976892.
[3] Ghannoum et al. "A Probiotic Amylase Blend Positively Impacts Gut Microbiota Modulation in a Randomized, Placebo-Controlled, Double-Blind Study." Life (Basel), 2024. DOI: 10.3390/life14070824. PMID: 39063578.
[4] Zaworski et al. "The Regulatory Role of Pancreatic Enzymes in the Maintenance of Small Intestinal Structure and Enterocyte Turnover with Special Reference to Alpha Amylase." Int J Mol Sci, 2024. DOI: 10.3390/ijms26010249. PMID: 39796104.
[5] Erta et al. "Salivary amylase activity: A potential modulator of glucose homeostasis, insulin secretion, and appetite regulation." Journal of Nutritional Biochemistry, 2026. DOI: 10.1016/j.jnutbio.2025.110154.
[6] Erta et al. "Salivary α-Amylase as a Metabolic Biomarker: Analytical Tools, Challenges, and Clinical Perspectives." Int J Mol Sci, 2025. DOI: 10.3390/ijms26157365. PMID: 40806495.
[7] Mandel & Breslin. "High endogenous salivary amylase activity is associated with improved glycemic homeostasis following starch ingestion in adults." Journal of Nutrition, 2012. DOI: 10.3945/jn.111.156984. PMID: 22492122.
스폰서 콘텐츠 안내: 이 글은 닥터블릿의 제품 정보를 바탕으로 작성된 분석 콘텐츠입니다. 편집팀은 독립적 검증을 거쳐 객관성을 유지합니다.
본 콘텐츠는 학술 논문과 공개된 연구 자료를 바탕으로 작성된 정보성 글이며, 의학적 진단이나 치료를 대체하지 않습니다. 건강 관련 결정은 반드시 담당 의료진과 상담하시기 바랍니다.