
하시모토 갑상선염(Hashimoto's thyroiditis)을 진단받은 후 식단 변화를 고민하는 경우가 많습니다. 글루텐을 끊으면 항체 수치가 낮아진다는 이야기, 요오드를 줄여야 한다는 조언이 온라인에 자주 등장합니다. 이 글은 현재까지 발표된 임상 연구를 바탕으로, 그 근거가 어느 정도이고 어떤 조건에서 의미가 있는지를 차분하게 살펴봅니다.
하시모토 갑상선염은 면역계가 갑상선 조직을 공격하는 자가면역 질환(autoimmune disease)입니다. 갑상선 과산화효소(thyroid peroxidase, TPO)와 티로글로불린(thyroglobulin, TG)에 대한 자가항체가 만들어지고, 이 과정이 지속되면 갑상선 기능이 저하됩니다. 치료의 주축은 레보티록신(levothyroxine) 같은 호르몬 보충 요법입니다.
식단이 자가면역 반응에 영향을 줄 수 있다는 생각은 여러 경로에서 나옵니다. 장내 환경이 면역 조절에 관여한다는 연구들이 늘면서, 특정 식품이 장 투과성(intestinal permeability)을 높이거나 낮출 수 있다는 가설이 제기되었습니다. 하시모토 갑상선염에서 주목받는 식이 요인은 크게 두 가지입니다. 글루텐(gluten)과 요오드(iodine)입니다.
두 요인 모두 기전 가설이 있고, 일부 임상 연구가 존재합니다. 그러나 연구 규모가 작고 결과가 일관되지 않아, 현재 기준으로 보편적 권고가 이루어지지 않는 상태입니다. 2023년 Nutrients 저널에 발표된 체계적 문헌 고찰(systematic review)은 1,350편을 검토해 9개 연구를 분석했는데, 글루텐·유당·에너지 제한이 항-TPO, TSH, fT4에 개선 효과를 보였지만 요오드 제한은 포함된 단일 연구에서 유의미한 개선이 없었다고 보고했습니다[2].
이처럼 연구 결과는 단순하지 않습니다. 효과가 전혀 없다고 단정하기도 어렵고, 모든 환자에게 권장할 수준도 아닙니다. 중요한 것은 어떤 환자에게, 어떤 조건에서 의미가 있는지를 구분하는 일입니다. A씨는 하시모토 갑상선염 진단 후 온라인 정보를 보고 글루텐을 전면 제한했지만, 3개월 후 피로감이 오히려 심해졌습니다. 이후 주치의와 상담하면서 철분과 B군 비타민 결핍이 원인이었음을 알게 되었습니다. 식단 변화가 의도치 않은 결과를 낳을 수 있다는 점을 보여주는 사례입니다.
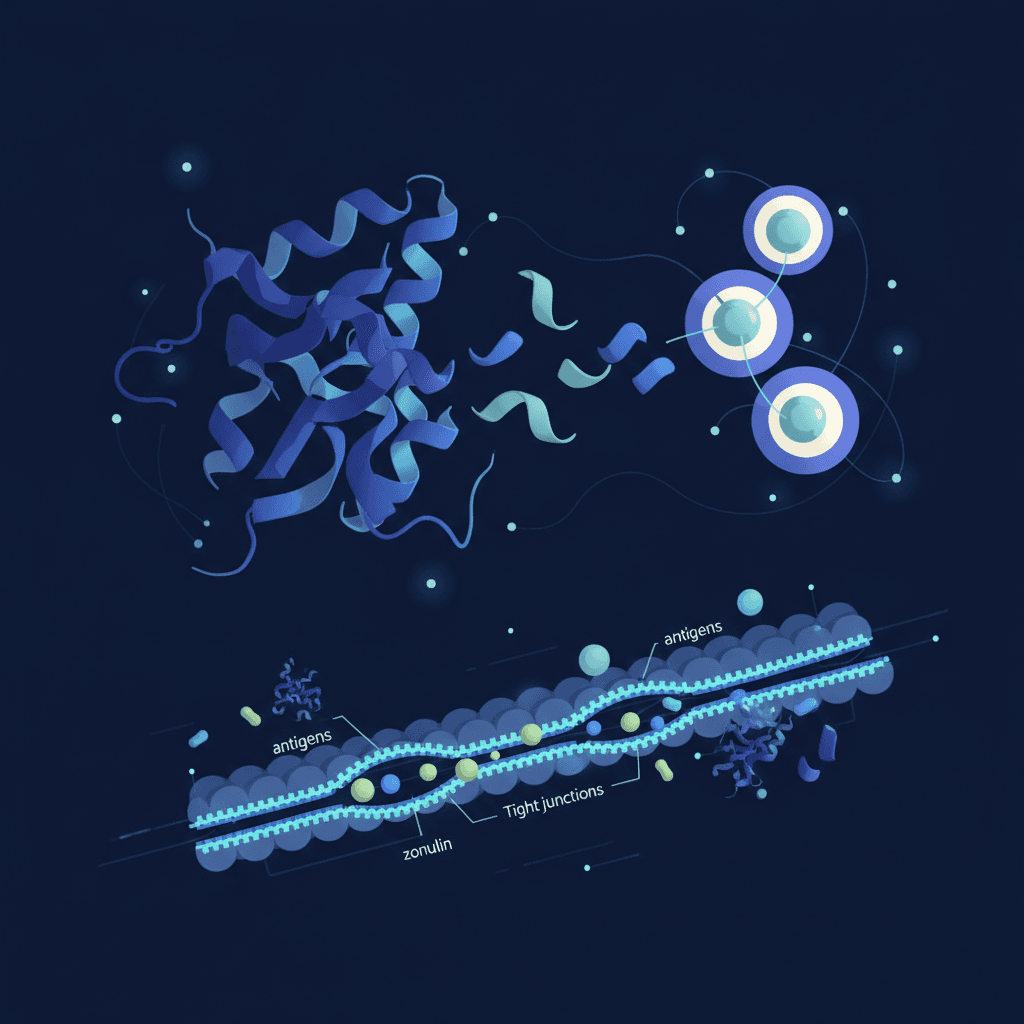
글루텐 제한(gluten-free diet, GFD)이 하시모토 갑상선염에 영향을 미칠 수 있다는 가설은 분자 유사성(molecular mimicry) 개념에서 시작됩니다. 글루텐의 구성 단백질인 글리아딘(gliadin)이 갑상선 트랜스글루타미나제(thyroid transglutaminase)나 TPO와 구조적으로 유사해, 글리아딘에 대한 면역 반응이 갑상선 항원을 교차 공격할 수 있다는 설명입니다[7]. 여기에 조눌린(zonulin)이 장 상피 세포의 밀착연접(tight junction)을 느슨하게 만들어 장 투과성을 높이고, 항원 노출을 증가시킬 수 있다는 기전도 함께 논의됩니다.
임상 증거를 보면, 2023년 Frontiers in Endocrinology에 발표된 메타분석(meta-analysis)이 가장 높은 근거 수준을 제공합니다. 이 연구는 글루텐 무감수성(celiac disease)이 없는 하시모토 갑상선염 환자에게 약 6개월간 글루텐 제한 식단을 적용한 연구들을 분석했습니다. 항-TgAb는 효과 크기(effect size) -0.39(p=0.06), 항-TPOAb는 ES -0.40(p=0.07)으로 감소 경향을 보였고, TSH는 ES -0.35(p=0.02)로 유의미하게 낮아졌으며 fT4는 ES +0.35(p=0.02)로 소폭 증가했습니다[1]. 통계적 유의성이 경계선에 걸쳐 있고, GRADE 기준으로 전반적 근거 수준이 낮다는 점이 주목됩니다.
12개월 추적 무작위 대조 시험(RCT)에서는 글루텐 제한군(n=62)에서 TSH가 유의미하게 감소했지만(p<0.05), 항-TPO나 항-TG 수치에는 유의미한 변화가 없었습니다[3]. 6개월 파일럿 연구(n=34, 전원 항-tTG 양성)에서는 글루텐 민감성이 확인된 하위 집단에서 항체 수치가 감소했습니다[4]. 종합하면, 이익이 가장 명확하게 나타나는 집단은 셀리악병(celiac disease) 또는 비셀리악 글루텐 과민성이 확인된 환자들입니다. 자가면역 갑상선 질환 환자에서 생검으로 확인된 셀리악병 유병률은 1.6%(95% CI 1.3~1.9%)로 일반 인구보다 높지만, 대다수 환자는 이 범주에 해당하지 않습니다[8].
글루텐 제한 식단의 잠재적 위험도 간과하기 어렵습니다. 정제된 글루텐 프리 가공식품은 B군 비타민, 철분, 셀레늄(selenium), 아연(zinc) 함량이 낮은 경우가 많아 영양 결핍을 유발할 수 있습니다[7]. B씨는 하시모토 갑상선염으로 글루텐 제한 식단을 6개월간 이어갔습니다. 항체 수치는 큰 변화가 없었고, 혈액검사에서 엽산과 철분이 기준치 아래로 내려갔습니다. 식단 변화가 목표했던 항체 감소보다 다른 결핍을 먼저 일으킨 경우입니다. 글루텐 민감성이 확인되지 않은 상황에서 글루텐 제한을 시작할 때는 영양 상태를 함께 모니터링하는 것이 중요한 이유입니다.
현재 근거를 종합하면, 글루텐 제한 식단은 셀리악병 또는 항-tTG 항체 양성인 하시모토 갑상선염 환자에서 일부 유익을 기대할 수 있습니다. 이 조건이 없는 환자에게 보편적으로 적용하기에는 근거가 충분하지 않습니다.
요오드는 갑상선 호르몬 합성에 필수적인 미량 원소입니다. 결핍되면 갑상선 기능 저하와 갑상선종(goiter)이 생기고, 과잉되면 특히 자가면역 소인이 있는 사람에서 갑상선 기능에 문제를 일으킬 수 있습니다. 이 역설적 관계가 요오드와 하시모토 갑상선염의 연결 고리입니다.
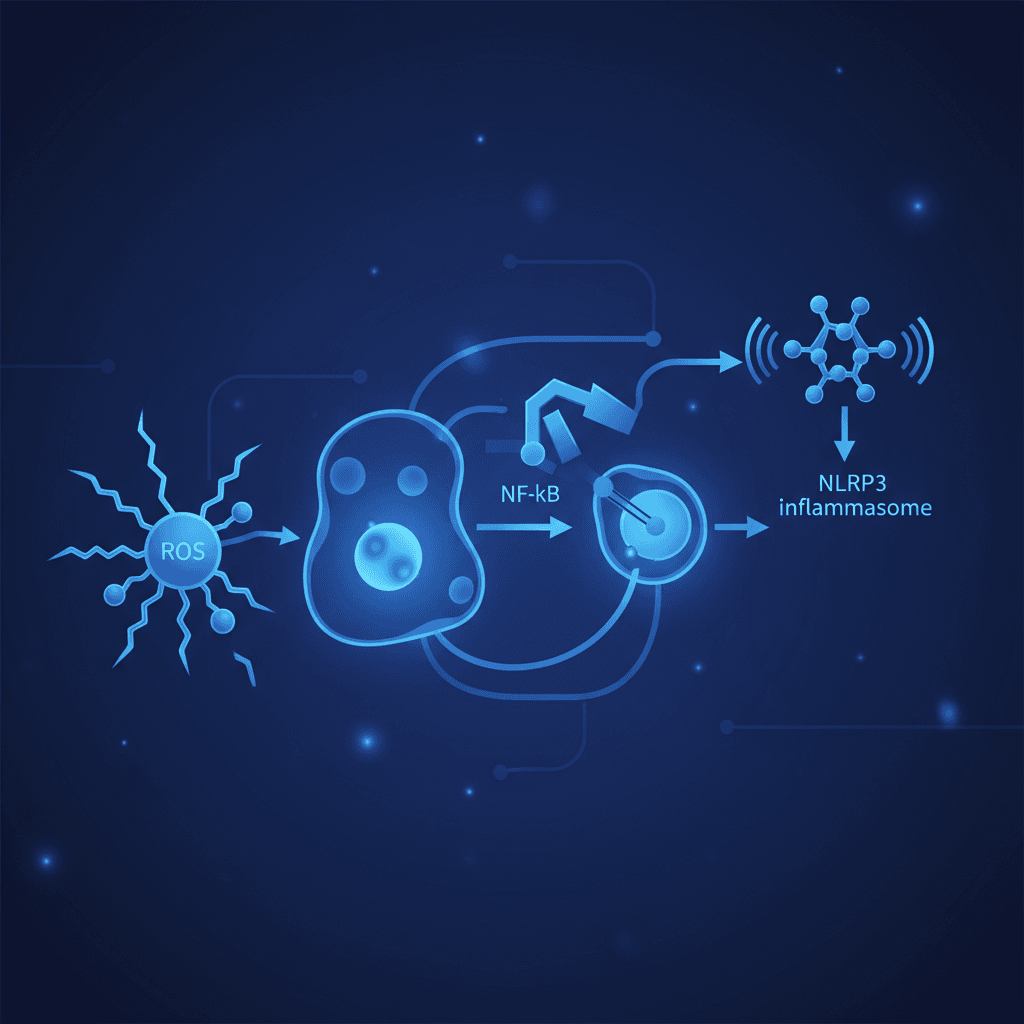
기전 측면에서, 과잉 요오드는 활성산소종(reactive oxygen species, ROS)을 생성해 NF-κB 경로를 활성화하고, NLRP3 염증소체(inflammasome)를 통해 갑상선 여포 상피세포의 파이롭토시스(pyroptosis, 염증성 세포사)를 유발합니다. 이 과정에서 IL-1β 같은 염증성 사이토카인이 방출되어 자가면역 염증이 지속됩니다[6]. 셀레늄은 글루타티온 퍼옥시다제(glutathione peroxidase) 등의 항산화 효소 구성 성분으로, 요오드로 인한 산화 손상을 완충하는 역할을 합니다[6][7].
임상 근거로는 2003년 Yonsei Medical Journal에 발표된 RCT가 중요한 참고점입니다. 요오드 과잉 섭취가 확인된 하시모토 갑상선염 관련 갑상선 기능 저하증 환자(n=45)를 대상으로, 요오드 제한(<100 µg/일, 3개월) 후 정상 갑상선 기능 회복률이 78.3%로, 비제한군의 45.5%보다 유의미하게 높았습니다[5]. 회복을 예측한 인자는 초기 TSH가 낮고 소변 요오드 농도가 높은 경우, 즉 요오드 과잉 상태가 명확했던 환자들이었습니다. 다시 말해, 이 연구의 혜택은 요오드 과잉이 확인된 집단에 집중되었습니다.
반면, 체계적 문헌 고찰에서 포함된 단일 요오드 제한 연구는 유의미한 개선을 보여주지 못했습니다[2]. 요오드 섭취량이 이미 적절한 수준인 환자에게 추가 제한을 적용하는 것은 근거가 부족하고, 오히려 요오드 결핍을 유발할 위험이 있습니다. 레보티록신을 복용하는 환자에서 요오드 제한을 적용할 경우 갑상선 호르몬 균형이 달라질 수 있어 용량 조정이 필요할 수 있습니다[5].
정리하면, 요오드 제한이 의미를 가지는 상황은 소변 요오드 검사 등을 통해 요오드 과잉이 객관적으로 확인된 경우로 한정됩니다. 일반적인 한국 식단에서 요오드 섭취 수준은 개인차가 크고, 과잉 여부는 검사 없이 판단하기 어렵습니다. 해조류 섭취가 많거나 요오드 강화 식품을 다량 섭취하는 경우에는 의료진과 함께 섭취량을 평가해 볼 수 있습니다.
식단 변화는 약물 치료를 대체하지 않습니다. 하시모토 갑상선염의 일차 치료는 갑상선 기능 저하가 동반된 경우 레보티록신 보충입니다. 식단 조정은 보조적인 접근으로, 일부 환자에서 항체 수치나 갑상선 기능 지표에 긍정적 영향을 줄 가능성이 있지만, 모든 환자에게 같은 결과가 나타나지는 않습니다.
글루텐 제한을 고려하는 경우, 먼저 셀리악병 및 비셀리악 글루텐 민감성(non-celiac gluten sensitivity, NCGS) 여부를 확인하는 검사가 선행되는 것이 합리적입니다. 항-tTG IgA 검사와 함께 임상 증상(소화 장애, 피부 증상 등)을 종합적으로 평가합니다. 검사에서 음성이고 증상도 없는 경우, 글루텐 제한의 근거는 현저히 약해집니다. 만약 식단 변화를 시작한다면 B군 비타민, 철분, 셀레늄, 아연 수치를 정기적으로 모니터링하는 것이 중요합니다[7].
셀레늄은 요오드 대사와 갑상선 자가면역 모두에 관여하는 영양소로, 하시모토 갑상선염 환자에서 보충이 일부 근거를 갖는 영양소입니다. 요오드로 인한 산화 손상을 완충하고[6], 글루텐 제한 식단과 병행 시 비타민 D 수치 증가가 관찰된 연구도 있습니다[4]. 다만 셀레늄도 과잉 섭취 시 독성이 있어 용량은 반드시 의료진과 상의해야 합니다.
요오드 제한을 고려하는 경우, 소변 요오드 농도 측정을 통해 현재 섭취 수준을 객관적으로 파악하는 것이 출발점입니다. 요오드 과잉이 확인되지 않은 상태에서 무조건 줄이는 것은 이득보다 해가 클 수 있습니다. 레보티록신 복용 중이라면 식단 변화 후 갑상선 기능 검사를 통해 호르몬 수준을 재확인하는 것이 안전합니다[5].
식단 변화의 효과는 개인차가 크고, 단기간에 항체 수치가 극적으로 달라지는 경우는 드뭅니다. 충분한 기간을 두고 혈액 검사를 통해 변화를 추적하면서, 영양 결핍이 생기지 않도록 균형을 유지하는 것이 장기적으로 더 안전한 접근입니다.
Q. 하시모토 갑상선염이 있으면 무조건 글루텐을 끊어야 하나요?
현재 근거로는 셀리악병 또는 비셀리악 글루텐 민감성이 확인되지 않은 환자에게 글루텐 제한을 보편적으로 권고하기에는 충분하지 않습니다[1][7]. 검사 없이 시작하는 경우 영양 결핍 위험이 있어, 의료진과 상담 후 검사 결과를 바탕으로 결정하는 것이 합리적입니다.
Q. 요오드가 많은 음식을 완전히 피해야 하나요?
요오드가 자가면역 반응에 영향을 줄 수 있다는 기전 연구는 있지만[6], 임상적으로 요오드 제한이 유익한 경우는 요오드 과잉이 객관적으로 확인된 환자로 한정됩니다[5]. 해조류를 일상적으로 다량 섭취하는 경우가 아니라면 소변 요오드 검사로 현재 상태를 먼저 파악하는 것이 선행됩니다.
Q. 항-TPO 수치가 높은데 식단으로 낮출 수 있나요?
식단 변화가 항체 수치에 영향을 줄 가능성은 있지만, 효과 크기가 작고 개인차가 큽니다. 메타분석에서 항-TPOAb 감소 효과 크기는 -0.40(p=0.07)으로 통계적 경계 수준이었습니다[1]. 항체 수치는 갑상선 기능 상태와 함께 종합적으로 해석되어야 하며, 항체 수치만을 목표로 식단을 극단적으로 변화시키는 것은 다른 문제를 일으킬 수 있습니다.
Q. 셀레늄 보충제가 도움이 되나요?
셀레늄은 갑상선 호르몬 대사와 산화 방어에 관여해, 하시모토 갑상선염에서 일부 연구에서 항체 감소와 연관된 결과를 보였습니다[6][7]. 그러나 셀레늄 과잉은 독성이 있고, 적정 용량은 개인의 기저 수준에 따라 다릅니다. 혈청 셀레늄 수치를 확인한 후 의료진의 판단에 따라 접근하는 것이 안전합니다.
Q. 글루텐 제한과 요오드 제한을 동시에 시도해도 되나요?
두 가지를 동시에 시작하면 어느 쪽이 효과를 냈는지 파악하기 어렵고, 식단이 지나치게 제한되어 영양 불균형이 생길 위험이 높아집니다. 한 번에 하나씩 충분한 관찰 기간(최소 3~6개월)을 두고 혈액 검사를 병행하며 진행하는 방식이 결과를 평가하기에 더 유리합니다.
[1] Piticchio T et al. "Effect of gluten-free diet on autoimmune thyroiditis progression in patients with no symptoms or histology of celiac disease: a meta-analysis." Frontiers in Endocrinology (Lausanne), 2023. DOI: 10.3389/fendo.2023.1200372. PMID: 37554764.
[2] Osowiecka K & Myszkowska-Ryciak J. "The Influence of Nutritional Intervention in the Treatment of Hashimoto's Thyroiditis—A Systematic Review." Nutrients, 2023; 15(4):1041. DOI: 10.3390/nu15041041. PMID: 36839399.
[3] Pobłocki J et al. "Whether a Gluten-Free Diet Should Be Recommended in Chronic Autoimmune Thyroiditis or Not?—A 12-Month Follow-Up." Journal of Clinical Medicine, 2021; 10(15):3240. DOI: 10.3390/jcm10153240. PMID: 34362024.
[4] Krysiak R, Szkróbka W, Okopień B. "The Effect of Gluten-Free Diet on Thyroid Autoimmunity in Drug-Naïve Women with Hashimoto's Thyroiditis: A Pilot Study." Experimental and Clinical Endocrinology & Diabetes, 2019. DOI: 10.1055/a-0653-7108. PMID: 30060266.
[5] Yoon SJ et al. "The effect of iodine restriction on thyroid function in patients with hypothyroidism due to Hashimoto's thyroiditis." Yonsei Medical Journal, 2003; 44(2):227-235. DOI: 10.3349/ymj.2003.44.2.227. PMID: 12728462.
[6] Liu X et al. "Excessive Iodine Promotes Pyroptosis of Thyroid Follicular Epithelial Cells in Hashimoto's Thyroiditis Through the ROS-NF-κB-NLRP3 Pathway." Frontiers in Endocrinology, 2019; 10:778. DOI: 10.3389/fendo.2019.00778. PMID: 31824415.
[7] Ihnatowicz P, Wątor P, Drywień ME. "The importance of gluten exclusion in the management of Hashimoto's thyroiditis." Annals of Agricultural and Environmental Medicine, 2021; 28(4):558-568. DOI: 10.26444/aaem/136523. PMID: 34969211.
[8] Roy A et al. "Prevalence of Celiac Disease in Patients with Autoimmune Thyroid Disease: A Meta-Analysis." Thyroid, 2016; 26(6):880-890. DOI: 10.1089/thy.2016.0108. PMID: 27256300.
본 콘텐츠는 학술 논문과 공개된 연구 자료를 바탕으로 작성된 정보성 글이며, 의학적 진단이나 치료를 대체하지 않습니다. 건강 관련 결정은 반드시 담당 의료진과 상담하시기 바랍니다.