
혈당 스파이크 예방 전략은 당뇨병 환자뿐 아니라 건강한 성인에게도 중요한 과제입니다. 식사 후 혈당이 급격히 오르내리는 이 현상은 최근 10년 사이 발표된 임상 연구들을 통해 새롭게 조명되고 있습니다. 연구들은 무엇을 먹느냐만큼이나 어떤 순서로 먹느냐가 식후 혈당 곡선에 결정적인 영향을 미친다는 사실을 보여주고 있습니다. 이 글은 그 근거들을 정리하고, 일상에서 적용할 수 있는 식사 전략을 소개합니다.

혈당 스파이크(blood sugar spike)란 식사 후 혈중 포도당 농도가 빠르게 상승했다가 급격히 떨어지는 현상을 가리킵니다. 건강한 성인의 경우 식사 후 혈당은 통상 60~90분 사이에 최고점에 도달한 뒤 서서히 기저치로 돌아옵니다. 그런데 정제 탄수화물이나 당분이 많은 음식을 빠르게 섭취하면 이 곡선이 훨씬 가팔라집니다.
이 현상이 문제가 되는 이유는 크게 두 가지입니다. 첫째, 혈당이 빠르게 오르면 췌장은 그에 대응하기 위해 인슐린(insulin)을 대량 분비하고, 이 인슐린이 혈당을 과도하게 낮추면서 식곤증, 집중력 저하, 허기 재발 등의 증상으로 이어질 수 있습니다. 둘째, 이러한 혈당 변동이 반복되면 인슐린 저항성(insulin resistance) 발생 위험이 높아지고, 장기적으로 제2형 당뇨병(type 2 diabetes mellitus, T2DM) 및 심혈관 질환으로 이어질 수 있다는 연구가 축적되어 있습니다.
40대 직장인 A씨는 점심에 흰쌀밥과 국, 반찬을 빠른 속도로 먹고 나면 오후 2시가 되기 전에 심한 졸음과 집중력 저하를 경험한다고 말했습니다. 이는 식후 혈당 스파이크와 그에 따른 반응성 저혈당(reactive hypoglycemia)의 전형적인 패턴에 해당합니다. 혈당 모니터링 기기가 대중화되면서 이처럼 자신의 혈당 패턴을 인식하는 사람이 늘어나고 있습니다.
특히 당뇨 전단계(prediabetes) 혹은 T2DM을 이미 진단받은 경우, 식후 고혈당 반응은 장기적인 합병증 위험과 직결됩니다. 망막병증, 신장 기능 저하, 말초신경병증 등 당뇨 합병증은 만성적인 혈당 상승이 축적될 때 발생합니다. 혈당 스파이크 예방 가능성을 식사 순서와 음식 조합으로 검증한 임상 연구들이 주목받는 배경입니다.
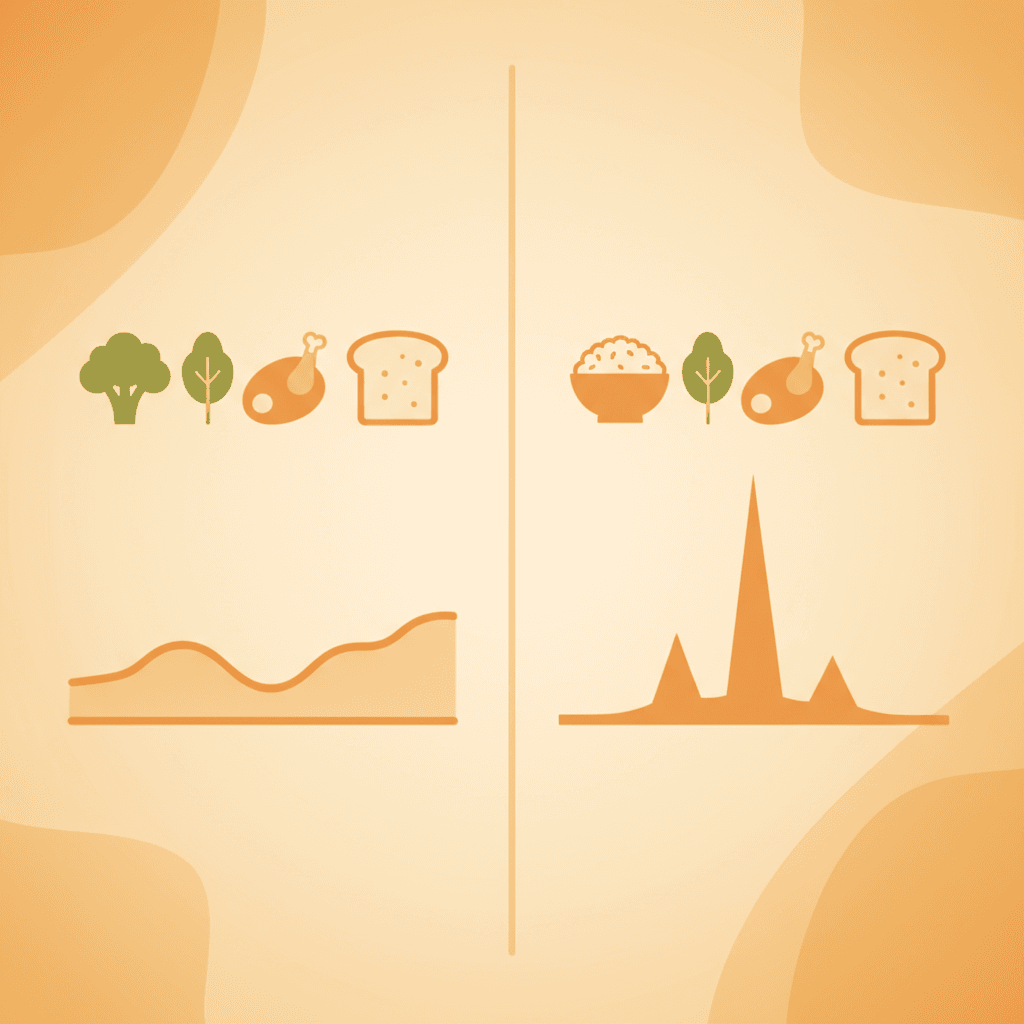
식사 순서가 혈당에 미치는 영향을 가장 직접적으로 보여준 연구 중 하나는 Shukla 등이 2015년 《Diabetes Care》에 발표한 무작위 대조 교차 시험(randomized controlled crossover trial)입니다. T2DM 환자 11명을 대상으로 채소와 단백질을 먼저 먹고 탄수화물을 마지막에 먹는 조건과, 탄수화물을 먼저 먹는 조건을 비교했을 때, 탄수화물을 마지막에 먹은 조건에서 식후 혈당 증가면적(incremental area under the curve, iAUC)이 73% 감소했으며, 혈당 피크도 36.7% 낮았습니다. 인슐린 iAUC 역시 48.5% 낮게 나타났습니다(p=0.002). [2]
같은 연구팀은 2017년 《BMJ Open Diabetes Research & Care》에 더 규모를 키운 후속 연구를 발표했습니다. 이번에는 T2DM 환자 16명을 대상으로 탄수화물 마지막 섭취 조건과 탄수화물 먼저 섭취 조건을 비교했는데, 탄수화물 마지막 조건에서 혈당 iAUC가 53%, 혈당 피크가 54% 낮아졌습니다(각각 p<0.001). 이와 함께 글루카곤 유사 펩타이드-1(glucagon-like peptide-1, GLP-1) 분비도 유의하게 증가했습니다(p=0.019). [3] GLP-1은 췌장의 인슐린 분비를 자극하고 위 배출 속도를 늦추는 인크레틴(incretin) 호르몬으로, 식후 혈당 안정화에 핵심적인 역할을 합니다.
당뇨 전단계 환자를 대상으로 한 연구에서도 유사한 결과가 확인되었습니다. Shukla 등은 2019년 당뇨 전단계 성인 15명을 대상으로 3가지 식사 순서를 비교한 교차 시험에서 단백질-채소 먼저 섭취 조건이 탄수화물 먼저 조건 대비 혈당 iAUC를 38.8% 줄이고, 혈당 피크를 40% 이상 낮췄다고 보고했습니다(p<0.05). [4] 건강한 성인을 대상으로 한 연구에서도 채소-육류-밥 순서(V-M-R 시퀀스)가 식후 60분 이내 인슐린 수치를 가장 낮게 유지하면서 GLP-1을 가장 높게 유지했습니다. 순서×시간 상호작용은 통계적으로 유의했습니다(P<0.001). [5]
이러한 개별 연구들의 결과는 체계적 문헌 고찰(systematic review)을 통해서도 일관되게 확인됩니다. Ferguson과 Wilson이 2023년 《Journal of the American Nutrition Association》에 발표한 고찰에 따르면, 검토 대상 11개 연구 전부에서 탄수화물을 마지막에 먹는 조건이 식후 혈당 및 인슐린 수치 감소와 연관되었으며, GLP-1 역시 탄수화물 마지막 조건에서 높게 나타났습니다. [1]
식사 순서 외에도 음식 조합 자체가 혈당 반응을 조절하는 데 중요한 역할을 합니다. 핵심은 혈당지수(glycemic index, GI)와 식이섬유(dietary fiber) 섭취입니다. GI란 특정 음식이 혈당을 얼마나 빠르게 올리는지를 포도당 기준 100으로 나타낸 지표입니다. 흰쌀밥이나 흰 빵처럼 정제된 탄수화물은 GI가 높고, 현미, 귀리, 콩류처럼 가공이 덜 된 식품은 GI가 낮습니다. 낮은 GI 식품을 선택하는 것이 식후 혈당 급등을 완화하는 기본 전략입니다.
수용성 식이섬유(soluble dietary fiber)는 혈당 조절에 특히 주목할 만한 성분입니다. 베타글루칸(beta-glucan), 사일리움(psyllium), 글루코만난(glucomannan) 등의 수용성 섬유는 소화관 내에서 점성이 높은 젤 형태를 형성하여 포도당의 흡수 속도를 물리적으로 늦춥니다. Vlachos 등이 2020년 《Nutrients》에 발표한 체계적 문헌 고찰에 따르면, 탄수화물 총량을 줄이거나 수용성 섬유 섭취를 늘리는 것이 T2DM 환자의 식후 혈당을 유의하게 개선한다고 보고했으며, 검토된 대부분의 임상 시험에서 p<0.05 수준의 유의한 결과가 도출되었습니다. [7]
단백질(protein)과 지방(fat)의 역할도 간과할 수 없습니다. 단백질은 콜레시스토키닌(cholecystokinin, CCK)과 펩타이드 YY(peptide YY, PYY)라는 호르몬 분비를 자극하여 위 배출 속도를 늦추고, 이로 인해 탄수화물이 십이지장에 도달하는 속도가 느려집니다. 쉽게 말해, 단백질 식품을 먼저 먹으면 소화 경로 자체가 탄수화물 흡수의 '브레이크' 역할을 하게 됩니다. 건강한 성인 18명을 대상으로 한 Shaheen 등의 2024년 교차 시험에서는 채소-단백질-탄수화물 순서(VPF 시퀀스)가 표준 혼합 식사 대비 혈당 iAUC를 40.9%(p=0.03), 인슐린 iAUC를 31.7%(p=0.023) 줄였으며, 식후 120분 시점의 포만감도 유의하게 높았습니다(p=0.04). [6]
비전분성 채소(non-starchy vegetables), 즉 브로콜리, 시금치, 오이, 파프리카 등은 GI가 낮고 식이섬유 함량이 높아 첫 번째로 먹기에 적합합니다. 이어서 생선, 두부, 닭가슴살 등 단백질이 풍부한 식품을 먹고, 탄수화물은 낮은 GI 선택지(현미, 통곡물 빵, 콩류)로 마지막에 먹는 구성이 여러 연구에서 일관되게 효과적인 것으로 나타났습니다.

식사 순서와 음식 조합 전략을 일상에서 적용하는 방법은 단순합니다. 식사 시작 시 비전분성 채소를 먼저 먹고, 이어서 단백질 식품을 먹은 뒤 탄수화물을 마지막에 먹는 패턴이 핵심입니다. 외식 상황에서는 밥이나 면류보다 샐러드나 나물류를 먼저 먹고, 단백질 반찬을 다음에 먹는 방식으로 응용할 수 있습니다.
당뇨 전단계를 진단받은 50대 B씨는 식사 순서를 바꾼 뒤 2~3주 후 점심 식후 피로감이 눈에 띄게 줄었다고 했습니다. 이 사례가 임상 증거는 아니지만, 소개한 연구들의 메커니즘과 일치하는 경험입니다.
주의해야 할 안전 사항도 있습니다. 인슐린 주사나 경구 혈당강하제를 사용 중인 T2DM 환자라면 식사 순서를 갑자기 바꿀 경우 혈당이 예상보다 낮게 떨어질 가능성이 있습니다. 따라서 식사 방식을 크게 변경할 때는 담당 의료진과 사전에 상의하는 것이 중요합니다.
혈당 스파이크 예방 효과는 단일 전략보다 복합적인 접근에서 더 크게 나타납니다. 식사 순서를 지키면서 수용성 식이섬유가 풍부한 식품을 포함하고, 탄수화물은 낮은 GI 선택지를 고르는 것이 상호 보완적으로 작용합니다. 더 넓은 식이 전략은 식이섬유와 혈당 조절 글에서 확인할 수 있습니다.
결론적으로, 식사 순서를 채소와 단백질 먼저, 탄수화물 마지막으로 조정하는 전략은 T2DM 환자부터 건강한 성인까지 폭넓은 집단에서 식후 혈당 반응을 유의하게 줄이는 것으로 확인되어 있습니다. 먹는 순서와 조합을 조정하는 행동 기반 접근이라는 점에서 장기적인 지속 가능성도 높습니다. 낮은 GI 탄수화물 선택과 수용성 식이섬유 병행은 그 효과를 한층 강화합니다. 다만 약물 치료 중인 경우에는 반드시 의료진과 상의하여 개인 상황에 맞게 적용하는 것이 안전합니다.
Q1. 식사 순서를 바꾸면 얼마나 빨리 효과가 나타납니까?
A. 식사 순서 변경의 효과는 해당 식사에 즉각 나타납니다. 임상 연구들은 단일 식사 실험에서도 혈당 iAUC가 유의하게 낮아짐을 확인했습니다. 매 식사마다 순서를 지키는 것이 중요하며, 장기적인 혈당 지표 개선을 위해서는 꾸준한 습관화가 필요합니다.
Q2. 채소를 먼저 먹는 것이 어렵거나 입맛에 맞지 않는 경우 대안이 있습니까?
A. 비전분성 채소가 어렵다면, 콩류(두부, 낫토 등)나 해조류처럼 식이섬유와 단백질이 함께 풍부한 식품을 식사 초반에 배치하는 것도 유사한 효과를 기대할 수 있습니다. 핵심은 정제 탄수화물(흰밥, 빵, 면류)을 식사의 마지막 순서로 미루는 것입니다.
Q3. 당뇨 약을 복용 중인데 식사 순서를 바꿔도 됩니까?
A. 인슐린 주사나 경구 혈당강하제를 사용 중이라면 식사 방식을 크게 바꾸기 전에 담당 의사와 상의하는 것이 중요합니다. 약물이 현재 식사 패턴에 맞춰 처방된 경우, 혈당이 예상보다 낮아지는 상황이 발생할 수 있어 개별적인 조정이 필요합니다.
Q4. 혈당 스파이크 예방 관점에서 피해야 할 음식 조합이 있습니까?
A. 정제 탄수화물과 단순당을 식사 초반에 함께 먹는 것은 혈당 스파이크를 가장 빠르게 유발하는 패턴입니다. 식이섬유 없이 탄수화물만 단독으로 섭취하는 경우도 혈당 급등을 촉진합니다. 반대로 식이섬유, 단백질, 지방이 함께 포함된 식사는 혈당 반응을 완만하게 합니다.
Q5. GI 지수가 낮은 탄수화물을 먹으면 식사 순서를 지키지 않아도 됩니까?
A. 낮은 GI 탄수화물 선택과 식사 순서는 독립적으로 작용하는 전략입니다. GI가 낮은 현미나 통곡물을 선택하면서 식사 마지막에 먹는 순서를 지키면 효과가 상호 보완됩니다. 두 전략을 함께 적용할 때 혈당 반응 개선이 더 안정적인 경향이 있어, 어느 하나만 선택하기보다 조합하는 것이 합리적입니다.
Ferguson M, Wilson S. Ordered Eating and Its Effects on Various Postprandial Health Markers: A Systematic Review. Journal of the American Nutrition Association. 2023. DOI: 10.1080/27697061.2022.2161664. PMID: 36574255.
Shukla AP, et al. Food Order Has a Significant Impact on Postprandial Glucose and Insulin Levels. Diabetes Care. 2015. DOI: 10.2337/dc15-0429. PMID: 26106234.
Shukla AP, et al. Carbohydrate-last meal pattern lowers postprandial glucose and insulin excursions in type 2 diabetes. BMJ Open Diabetes Research & Care. 2017. DOI: 10.1136/bmjdrc-2017-000440. PMID: 28989726.
Shukla AP, et al. The impact of food order on postprandial glycaemic excursions in prediabetes. Diabetes, Obesity and Metabolism. 2019. DOI: 10.1111/dom.13503. PMID: 30101510.
Sun L, et al. Postprandial glucose, insulin and incretin responses differ by test meal macronutrient ingestion sequence (PATTERN study). Clinical Nutrition. 2020. DOI: 10.1016/j.clnu.2019.04.001. PMID: 31053510.
Shaheen N, et al. Postprandial Glucose and Insulin Response to Meal Sequence Among Healthy UAE Adults: A Randomized Controlled Crossover Trial. Diabetes, Metabolic Syndrome and Obesity. 2024. DOI: 10.2147/DMSO.S468628. PMID: 39559800.
Vlachos D, et al. Glycemic Index (GI) or Glycemic Load (GL) and Dietary Interventions for Optimizing Postprandial Hyperglycemia in Patients with T2 Diabetes: A Review. Nutrients. 2020. DOI: 10.3390/nu12061561. PMID: 32471238.
본 콘텐츠는 학술 논문과 공개된 연구 자료를 바탕으로 작성된 정보성 글이며, 의학적 진단이나 치료를 대체하지 않습니다. 건강 관련 결정은 반드시 담당 의료진과 상담하시기 바랍니다.