
위암은 초기 단계에서 뚜렷한 증상을 일으키지 않는 경우가 많습니다. 소화가 잘 안 되거나 속이 더부룩한 느낌이 오래 지속되더라도, 이를 단순한 소화불량으로 넘겨 검진 시기를 놓치는 사례가 반복됩니다. 이 글에서는 위암의 발생 기전과 초기 증상의 특성, 내시경 검진의 임상적 근거, 그리고 40세 이후 실질적인 검진 전략을 임상 연구 데이터를 중심으로 정리합니다.
위암(Gastric cancer)의 대부분을 차지하는 위선암(Gastric adenocarcinoma)은 점막층에서 시작되어 서서히 진행하는 특성을 가집니다. 점막층이나 점막하층에 국한된 조기 위암(Early gastric cancer) 단계에서는 신경 자극이 충분하지 않아 통증이나 출혈 같은 명확한 신호를 거의 만들어 내지 않습니다. 이 때문에 환자 스스로 무언가 잘못되었다는 것을 인식하기 어렵습니다.
상복부 불편감, 식욕 감소, 만성적인 소화불량(Dyspepsia)은 위암의 초기 증상으로 거론되기도 하지만, 이러한 증상들의 예측력은 생각보다 낮습니다. 소화불량이 위암 전구 병변을 예측할 수 있는지를 분석한 후향적 코호트 연구에서 3,699명을 대상으로 조사한 결과, 소화불량을 비롯한 고위험 증상들은 장상피화생(Intestinal metaplasia, GIM)이나 위암 전구 병변과 유의미한 연관성이 없었습니다(OR=1.0)[7]. 이 연구에서 유효한 위험 인자는 연령과 민족성이었습니다.
쉽게 말해, 증상이 없다고 해서 위 점막이 건강하다고 안심할 수 없고, 반대로 소화불량이 심하다고 해서 위암 전구 병변이 있다는 신호도 아닙니다. 증상이 위험을 알리는 역할을 하지 못한다는 것은, 다른 방법으로 위 점막 상태를 확인해야 한다는 것을 의미합니다.
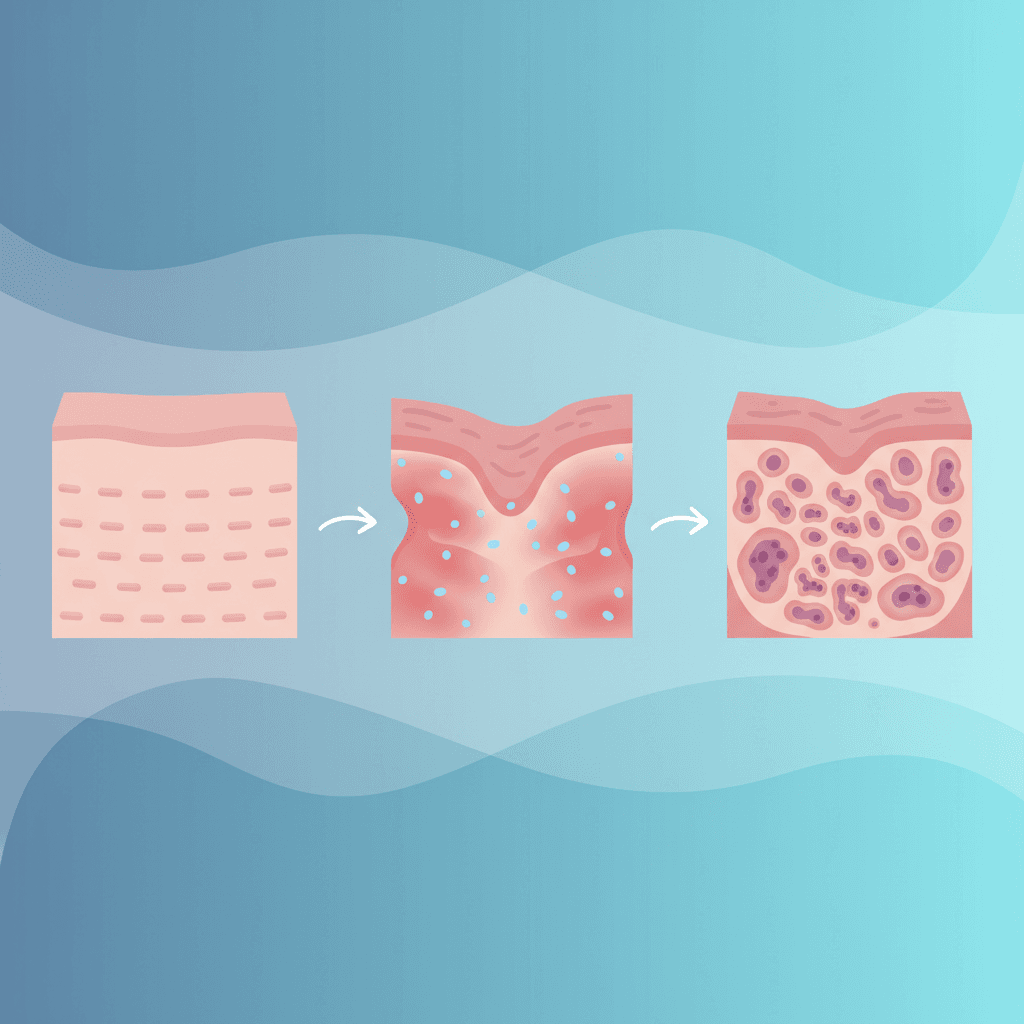
위암 발생의 주요 경로는 헬리코박터 파일로리(Helicobacter pylori, H. pylori) 감염에서 시작됩니다. H. pylori는 만성 위염(Chronic gastritis)을 유발하고, 이것이 수년에서 수십 년에 걸쳐 지속되면 위축성 위염(Atrophic gastritis)으로 진행합니다. 위축성 위염은 이후 장상피화생을 거쳐 이형성(Dysplasia)으로, 최종적으로는 침윤암으로 이어지는 단계적 변화를 따릅니다. 이 일련의 변화 과정을 코레아 계단식 모델(Correa cascade)이라고 부릅니다. 현재까지의 연구 결과에 따르면, 전 세계 위암의 약 89%에서 H. pylori 감염이 원인 인자로 확인됩니다.
이 경로의 특징은 증상 없이 조용히 진행된다는 점입니다. 위축성 위염 단계에서도, 장상피화생 단계에서도, 대부분의 환자는 일상 생활에서 특별한 불편감을 느끼지 않습니다. 그 결과, 검진을 받지 않은 상태에서는 이미 진행암으로 발전한 후에야 증상으로 병원을 찾게 되는 경우가 생깁니다. 이것이 증상 기반 접근법만으로는 조기 위암 발견에 한계가 있는 근본적인 이유입니다.
진행암 단계에서 나타나는 증상은 훨씬 구체적입니다. 체중 감소, 지속적인 구역감, 식사 후 포만감, 흑색변이나 혈변, 복부 종괴 촉지 같은 소견이 나타날 수 있습니다. 그러나 이 시점에서는 이미 암이 주변 조직이나 림프절로 퍼진 경우가 많아 완치를 목표로 하는 치료가 어려워집니다. 증상이 나타나고 나서야 검진을 받는 방식이 위험한 이유가 바로 이 간극에 있습니다. 조기 위암은 내시경 점막하 박리술(Endoscopic Submucosal Dissection, ESD)로도 완치가 가능한 반면, 3기 이상의 진행암에서는 수술, 항암화학요법, 방사선 치료를 복합적으로 시행해도 예후가 크게 나빠집니다.
내시경 검진(Endoscopic screening)의 효과는 대규모 메타분석 연구들을 통해 일관되게 확인됩니다. 44개 연구를 종합 분석한 체계적 문헌고찰에서, 내시경 검진의 조기 위암 발견율은 0.48%로 나타났으며, 이는 조영술(Upper GI series) 방식의 0.08%보다 유의하게 높은 수치입니다[3]. 조기에 발견할수록 치료 성적이 좋아지고, 생존율 향상으로 이어집니다.

사망률 감소 효과는 특히 주목할 만합니다. 총 1,667,117명을 대상으로 한 베이지안 메타분석(Bayesian meta-analysis) 연구에서, 내시경 검진 준수자는 비준수자에 비해 위암 사망률이 48% 낮았습니다. 구체적인 수치는 상대위험도(Relative Risk, RR)=0.52, 신뢰구간(Credible Interval, CrI) 0.39-0.79로 통계적으로 유의미했습니다[4]. 이 수치는 수백만 명 규모의 데이터를 통해 얻은 결과로, 내시경 검진의 효과를 가장 강력하게 뒷받침하는 근거 중 하나입니다.
검진 주기와 생존율의 관계도 실제 환자 데이터에서 확인됩니다. 위암 진단 환자 1,651명을 분석한 연구에서, 2년 이내에 내시경 검진을 받은 환자군은 진행암(Advanced gastric cancer)으로 발전할 위험이 32% 낮았습니다(OR=0.678)[6]. 1년 이내 검진 군에서는 이 위험 감소 폭이 49%로 더 컸습니다(OR=0.515)[6]. 검진 간격을 짧게 유지할수록 조기 발견 가능성이 높아진다는 것을 보여주는 수치입니다.
조영술과 내시경을 비교할 때, 내시경이 조기 발견율에서 우위를 보이는 이유는 검사의 특성에 있습니다. 조영술은 위 점막의 형태를 간접적으로 관찰하는 반면, 내시경은 점막 표면을 직접 시각화하고 필요 시 조직 생검(Biopsy)을 시행할 수 있습니다. 미세한 색조 변화나 함몰, 융기 같은 초기 변화를 직접 확인할 수 있다는 점이 내시경의 임상적 장점입니다.
이러한 근거를 토대로 국내 국가 암 검진 프로그램에서는 만 40세 이상 성인에게 2년 주기 위내시경 검진을 권고합니다. AGA(American Gastroenterological Association) 2025 가이드라인에서도 고위험군에 대한 내시경 선별을 권고하며, 위축성 위염이나 장상피화생이 확인된 경우에는 3년 주기 감시 내시경을 시행하도록 명시합니다[5].
일부에서는 내시경 검사 대신 혈액 검사나 위 기능 검사(Serum pepsinogen test)를 1차 선별 수단으로 활용하는 방식도 연구되고 있습니다. 혈청 펩시노겐(Serum pepsinogen) 검사는 위 점막 위축 정도를 간접적으로 반영하는 지표로, 특히 위축성 위염의 선별에 활용됩니다. 그러나 현재 임상 근거에서는 내시경이 조기 위암 발견의 정확도와 치료 연결성 측면에서 여전히 기준이 되는 검사입니다. 혈청 검사는 보완적 도구로서 의미가 있지만, 직접적인 점막 관찰을 대체하기에는 아직 증거가 부족한 상태입니다.
H. pylori 제균(Eradication) 치료는 위암의 상류 원인을 차단하는 전략입니다. 만성 염증이 지속되기 전에 감염원을 제거하면 코레아 계단식 변화의 첫 단계를 억제할 수 있습니다. 이것이 제균 치료를 내시경 검진과 함께 중요한 예방 수단으로 보는 이유입니다.
10개의 무작위 대조 시험(Randomized Controlled Trial, RCT)을 포함한 8,323명 대상의 메타분석에서, H. pylori 제균은 건강한 성인에서 위암 발생률을 46% 감소시켰습니다. 상대위험도는 RR=0.54, 95% 신뢰구간(Confidence Interval, CI) 0.40-0.72였습니다[1]. 치료 필요 수(Number Needed to Treat, NNT)는 72명으로, 72명을 제균 치료하면 1명의 위암 발생을 예방할 수 있다는 의미입니다. 또한 같은 메타분석에서 이미 위암 또는 전구 병변이 있는 환자군에서도 RR=0.49, NNT=21로 유의한 효과가 관찰되었습니다[1].
2025년에 발표된 최신 메타분석에서도 H. pylori 제균이 위암 위험을 36% 감소시킨다는 결과가 재확인되었습니다(RR=0.64; CI 0.48-0.84)[2]. 이처럼 두 개의 독립적인 고질 메타분석이 일관된 방향의 결과를 보여준다는 점은 제균 치료의 예방적 가치를 강하게 지지합니다.
단, 제균 치료의 예방 효과에는 중요한 조건이 있습니다. 장상피화생 단계 이전에 치료를 시행해야 효과가 더 뚜렷하게 나타납니다. 장상피화생이 이미 진행된 이후에는 제균을 하더라도 위암 억제 효과가 제한적인 것으로 알려져 있습니다[1]. 이는 검진을 통해 위 점막 상태를 먼저 확인하고, H. pylori 감염이 확인된 경우 가능한 한 이른 시점에 제균 치료를 시행하는 것이 예방 전략의 핵심임을 보여줍니다.
H. pylori 제균 요법은 일반적으로 2가지 항생제와 양성자 펌프 억제제(Proton Pump Inhibitor, PPI)를 병용하는 삼제 요법 또는 사제 요법으로 진행됩니다. 항생제 사용에 따라 오심과 설사 같은 경증 부작용이 10-30%에서 보고되지만, 대부분 일시적이며 치료 완료 후 소실됩니다[1][2]. 내시경 검사 자체도 드물게 천공(Perforation) 같은 합병증이 발생할 수 있으나, 그 빈도는 0.1% 미만으로 매우 낮은 수준입니다[3][4]. 위험 대비 이익의 비율을 고려할 때, 40세 이상 성인에게 정기 검진과 H. pylori 검사의 가치는 임상적으로 명확합니다.
한국의 H. pylori 감염률은 성인 기준으로 40-50% 수준으로 알려져 있어, 검진 과정에서 감염 여부를 확인하고 양성이면 제균 치료를 진행하는 것이 위암 예방 체계의 중요한 축이 됩니다. 제균 치료 후에는 요소 호기 검사(Urea Breath Test, UBT) 또는 대변 항원 검사(Stool Antigen Test)로 제균 성공 여부를 검증하는 것이 표준 절차입니다. 1차 제균에 실패한 경우에는 항생제 내성 패턴을 고려하여 다른 조합의 2차 제균 요법을 시행합니다. 제균 치료의 성공률은 1차 요법에서 약 70-90%, 2차 요법에서 추가로 개선됩니다.
검진 시작 시점은 40세를 기준으로 삼는 것이 국내외 권고의 공통된 방향입니다. 50세 이상에서는 장상피화생 위험이 급증한다는 관찰 데이터가 있으며[7], 40세에 검진을 시작하면 이 위험이 본격적으로 높아지기 전 단계에서 위 점막의 기저 상태를 파악할 수 있습니다. 첫 검진에서 이상 소견이 없다면 2년 주기가 기본 간격입니다.
위험 인자가 여러 개 복합적으로 존재하는 경우에는 더 짧은 검진 주기가 적합할 수 있습니다. H. pylori 양성이면서 직계 가족 중 위암 환자가 있는 경우, 또는 흡연과 고염식이를 병행하고 있는 경우라면 1년 주기의 검진이 권고될 수 있습니다[6]. 검진 주기의 결정은 개인의 위험 인자를 종합적으로 검토하는 담당 의료진의 판단이 중심이 되어야 합니다.

검진 결과에서 위축성 위염이나 장상피화생이 발견된다면, AGA 가이드라인은 3년 주기의 감시 내시경(Surveillance endoscopy)을 권고합니다[5]. 이는 병변이 이형성으로 진행하는 시점을 놓치지 않기 위한 안전망입니다. 특히 광범위한 장상피화생이 확인되거나 이형성의 증거가 있는 경우에는 더 짧은 간격의 추적 검사가 필요할 수 있으므로, 검진 후 결과에 대한 의료진의 설명을 주의 깊게 확인하는 것이 중요합니다.
가족력, 흡연, 고염식이, 가공육 섭취는 H. pylori 감염과 독립적인 위험 인자로 알려져 있습니다. 이러한 요인들이 복수로 해당된다면, 일반적인 권고 기준보다 더 이른 검진 시작을 고려하는 것이 현실적입니다. 위암 발생률이 높은 한국과 동아시아 지역에서는 소화기 계통에 대한 정기적인 모니터링을 만성질환 관리의 일환으로 접근하는 것이 바람직합니다.
내시경 검진에서 H. pylori 감염이 확인된 경우에는 제균 치료를 시행하고, 치료 완료 후 제균 성공 여부를 확인하는 것이 표준적인 절차입니다. 제균 성공 후에도 이미 진행된 위 점막 변화가 있다면 정기 검진은 계속 필요합니다. 제균 치료가 검진의 대체제가 아니라 보완적 수단이라는 점을 명확히 이해하는 것이 장기적인 예방 전략의 출발점입니다.
검진 받는 것 자체를 불편하게 느끼는 경우가 있습니다. 내시경 검사는 금식, 검사 전 처치, 검사 중 불편감이 수반되기 때문입니다. 수면 내시경이라고도 불리는 진정 내시경(Sedated endoscopy)은 이러한 부담을 크게 줄여줍니다. 경증 진정제를 사용하여 검사 중 불편감을 최소화하면서 점막을 충분히 관찰할 수 있습니다. 진정 내시경의 사용은 검진 수용률을 높이고 더 꼼꼼한 관찰을 가능하게 한다는 점에서 검진 효율 향상에도 기여합니다.
위암 관련 정보를 더 넓은 맥락에서 살펴보고 싶다면 위장 건강과 만성 소화기 질환 관리 가이드도 참고할 수 있습니다.
위암은 조기에 발견할수록 치료 성적이 현저히 좋아지는 암입니다. 뚜렷한 증상을 기다리는 방식으로는 조기 발견의 기회를 잡기 어렵습니다. 정기적인 내시경 검진과 H. pylori 검사 및 제균 치료가 현재 임상 근거가 지지하는 핵심 전략이며, 40세 이후라면 2년 주기 검진을 기본으로 삼고 개인의 위험 인자에 따라 담당 의료진과 구체적인 계획을 상의하는 것이 적절합니다.
Q. 위암 초기에 나타날 수 있는 증상은 무엇인가요?
조기 위암은 대부분 증상이 없습니다. 일부에서 상복부 불편감, 소화불량, 식욕 저하가 나타날 수 있지만, 이는 비특이적 증상으로 위암 전구 병변과의 관련성이 낮다는 연구 결과가 있습니다[7]. 증상의 유무와 관계없이 40세 이후 정기적인 내시경 검진이 중요한 이유가 여기에 있습니다.
Q. 위내시경 검진은 몇 살부터 시작해야 하나요?
국내 국가 암 검진 프로그램은 만 40세 이상에게 2년 주기의 위내시경 검진을 권고합니다. 가족력이 있거나 H. pylori 감염, 흡연, 고염식이 등 위험 인자가 복수로 확인된다면 더 이른 시작과 짧은 검진 주기를 담당 의료진과 상의하는 것이 적절합니다.
Q. H. pylori 제균 치료를 받으면 위암 예방에 도움이 되나요?
H. pylori 제균 치료는 건강한 성인에서 위암 발생률을 약 36-46% 감소시키는 것으로 메타분석에서 확인됩니다[1][2]. 단, 장상피화생이 이미 진행된 이후에는 효과가 제한적이므로, 감염이 확인되면 조기에 제균 치료를 시행하는 것이 더 효과적입니다.
Q. 위축성 위염이나 장상피화생 진단을 받으면 검진을 얼마나 자주 해야 하나요?
AGA 2025 가이드라인에 따르면, 위축성 위염이나 장상피화생이 확인된 경우에는 3년 주기의 감시 내시경을 시행하도록 권고합니다[5]. 병변의 범위나 이형성 여부에 따라 더 짧은 간격이 필요할 수 있으므로, 검진 결과를 담당 의료진과 충분히 확인하는 것이 중요합니다.
Q. 내시경 검진은 안전한가요?
내시경 검사는 전반적으로 안전한 시술입니다. 가장 심각한 합병증인 천공의 빈도는 0.1% 미만으로 매우 드뭅니다[3][4]. 검진으로 인한 위험보다 조기 위암 발견을 통해 얻는 이익이 훨씬 크다는 것이 현재 임상 근거의 방향입니다.
[1] Ford AC et al., "Helicobacter pylori eradication therapy to prevent gastric cancer: systematic review and meta-analysis," Gut, 2020. DOI: 10.1136/gutjnl-2020-320839
[2] Ford AC et al., "Eradication Therapy to Prevent Gastric Cancer in Helicobacter pylori-Positive Individuals," Gastroenterology, 2025. DOI: 10.1053/j.gastro.2024.12.033
[3] Faria M et al., "Gastric cancer screening: a systematic review and meta-analysis," Scandinavian Journal of Gastroenterology, 2022. DOI: 10.1080/00365521.2022.2068966
[4] Hibino M et al., "Radiographic and endoscopic screening to reduce gastric cancer mortality," Lancet Regional Health - Western Pacific, 2023. DOI: 10.1016/j.lanwpc.2023.100741
[5] Shah SC et al., "AGA Clinical Practice Update on Screening and Surveillance for Gastric Cancer in the United States," Gastroenterology, 2025. DOI: 10.1053/j.gastro.2024.11.001
[6] Kim GH et al., "Does the interval of screening endoscopy affect survival in gastric cancer patients?" Medicine, 2016. DOI: 10.1097/MD.0000000000005490
[7] Da JL et al., "High-risk symptoms do not predict gastric cancer precursors," Helicobacter, 2019. DOI: 10.1111/hel.12548
본 콘텐츠는 학술 논문과 공개된 연구 자료를 바탕으로 작성된 정보성 글이며, 의학적 진단이나 치료를 대체하지 않습니다. 건강 관련 결정은 반드시 담당 의료진과 상담하시기 바랍니다.