
혈액 한 번의 채혈로 50종 이상의 암을 동시에 스크리닝한다는 개념이 임상 현장에 가까워지고 있습니다. 다중암 조기검진 혈액검사(Multi-Cancer Early Detection, MCED)는 최근 수년간 대규모 전향적 연구 결과가 발표되면서 의학계의 주목을 받고 있는 분야입니다. 다만 높은 기대만큼 검증해야 할 과제도 적지 않으며, 현 시점에서 이 기술이 실제로 무엇을 할 수 있고 무엇을 아직 할 수 없는지를 정확히 이해하는 일이 중요합니다.

다중암 조기검진 혈액검사(MCED)의 핵심 원리는 혈액 속에 떠다니는 세포 유리 DNA(cell-free DNA, cfDNA)를 분석하는 데에 있습니다. 암세포는 정상 세포보다 빠르게 분열하고 사멸하면서 혈액으로 더 많은 DNA 조각을 방출하는데, 이 DNA의 메틸화(methylation) 패턴이 정상 조직과 다르다는 점을 이용합니다. 쉽게 말해, 특정 유전자 부위에 메틸기(-CH₃)가 붙어 있는 방식이 암 조직마다 독특한 지문처럼 남는다는 원리입니다.
2020년 Liu 등이 발표한 CCGA(Circulating Cell-free Genome Atlas) 컨소시엄 연구에서는 6,689명을 대상으로 cfDNA 메틸화 분석의 성능을 검증했습니다[1]. 이 연구에서 개발된 검사는 50종 이상의 암을 단일 혈액검사로 탐지하면서 특이도(specificity) 99.3%를 기록했습니다. 특이도가 높다는 것은 건강한 사람을 암이 아니라고 올바르게 판정하는 능력이 뛰어나다는 의미입니다.
암 신호(cancer signal)가 감지되면 검사는 암의 기원 조직(Cancer Signal Origin, CSO)도 함께 예측합니다. Liu 등의 연구에서 CSO 예측 정확도는 93%였습니다[1]. 이는 단순히 "암이 있다"는 사실을 알려주는 데 그치지 않고, 어느 장기에서 시작됐을 가능성이 높은지를 함께 제시함으로써 이후 정밀 검사의 방향을 안내할 수 있다는 점에서 중요한 의미를 가집니다.
머신러닝(machine learning) 알고리즘이 이 분석의 핵심 도구입니다. 수만 개의 메틸화 부위 데이터를 학습한 모델이 혈액 샘플에서 패턴을 감지하고, 이를 암 신호 유무 및 기원 조직 예측에 연결합니다. Imai 등의 2025년 종설에 따르면, 현재 상업적으로 가장 앞선 제품인 GRAIL Galleri와 CancerSEEK 모두 이와 같은 cfDNA 메틸화 기반 접근법을 채택하고 있습니다[3]. 기존의 단일 암 표지자 검사(예: PSA, CA-125)가 한 종류의 암에 특화되었다면, MCED는 하나의 플랫폼으로 여러 암 유형을 동시에 탐색하는 방식으로 작동합니다.

MCED 검사의 가장 주목받는 성능 지표는 병기별 민감도(sensitivity)입니다. Liu 등의 연구에서 Stage I(1기)의 민감도는 39%였으며, Stage II 69%, Stage III 83%, Stage IV에서는 92%까지 상승하는 양상이 확인되었습니다[1]. 이 수치는 기술의 가능성과 한계를 동시에 드러냅니다. 암이 이미 상당히 진행된 3~4기에서는 높은 탐지율을 보이지만, 조기 발견이 가장 중요한 1기에서는 10명 중 6명을 놓칠 수 있다는 의미이기도 합니다.
2025년 Wade 등이 발표한 체계적 문헌고찰(systematic literature review)은 36편의 연구를 종합하여 제품 간 성능 편차를 정리했습니다[5]. Galleri의 민감도는 20.8~66.3%, 특이도는 98.4~99.5% 범위였으며, CancerSEEK는 민감도 27.1~62.3%, 특이도 98.9~99.1%였습니다. 신흥 제품인 SPOT-MAS는 민감도 72.4~100%, 특이도 97.0~99.9%로 일부 연구에서 높은 수치를 보였으나, 연구 설계와 대상 암 종 구성에 따라 결과 편차가 크다는 점을 유의해야 합니다.
2023년 Schrag 등이 발표한 PATHFINDER 코호트 연구는 실제 임상 적용 가능성을 평가한 대표적인 전향적 연구입니다[2]. 50세 이상 무증상 성인 6,621명을 대상으로 한 이 연구에서 MCED 양성률은 1.4%(92명)이었으며, 양성 예측도(Positive Predictive Value, PPV)는 43.1%였습니다. 이는 양성 판정을 받은 사람 중 실제 암이 확인된 비율이 43.1%라는 의미로, 나머지 약 57%는 위양성(false positive)이었다는 뜻입니다.
2025년 Marinac 등의 실세계 연구는 미국 실제 임상 환경에서 111,080명에게 Galleri 검사를 시행한 결과를 분석했습니다[7]. 암 신호 검출률은 0.91%(1,011명)였고, PPV는 56.2%로 PATHFINDER 연구보다 다소 높았습니다. 32종의 암이 검출되었으며, CSO 정확도는 87%, 양성 판정 후 진단까지 걸린 중앙값은 39.5일이었습니다. 이 연구는 실제 진료 현장에서의 수행 능력을 보여준다는 점에서 의미가 있지만, 대조군이 없는 관찰 연구라는 설계상 한계도 함께 지닌다는 점은 주의가 필요합니다.
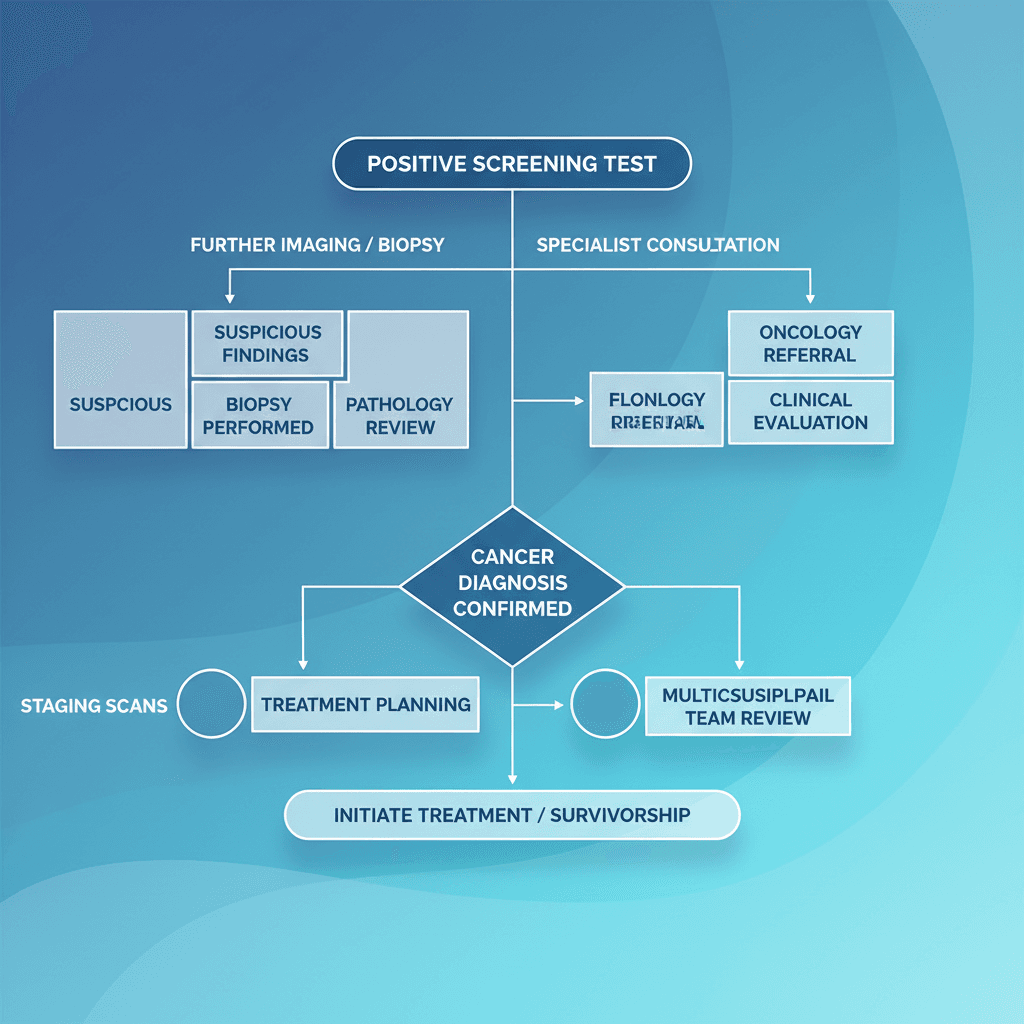
MCED 검사의 가장 실질적인 우려는 위양성(false positive) 문제입니다. PATHFINDER 연구에서 위양성률은 62%였으며, 위양성으로 판명되기까지 걸린 시간의 중앙값은 162일이었습니다[2]. 이는 암이 아님에도 불구하고 약 5개월간 추가 검사와 심리적 불안을 감당해야 할 수 있다는 것을 의미합니다. 위양성이 환자에게 미치는 정신적·경제적 부담은 검사의 임상적 순효과를 평가할 때 반드시 함께 고려해야 합니다.
2025년 Wan, Sasieni, Rosenfeld의 Nature Reviews Clinical Oncology 종설은 현재 진행 중인 대규모 무작위대조시험(Randomized Controlled Trial, RCT)들이 결과를 내놓기 전까지 1세대 MCED 검사의 임상적 유익성은 아직 증명되지 않았다고 명시합니다[4]. 검사가 암을 조기에 발견한다 하더라도, 이것이 실제 사망률 감소로 이어지는지를 확인하는 것은 별개의 문제입니다. 진단 시점이 앞당겨지지만 치료 결과가 달라지지 않는 리드타임 바이어스(lead-time bias)의 가능성도 배제할 수 없습니다.
비용과 접근성 문제도 현실적인 장벽입니다. 현재 Galleri의 검사 비용은 약 949달러(USD)이며, 미국의 주요 보험사는 대부분 급여 적용을 하지 않고 있습니다[3][4]. 이는 검사 이용이 경제적으로 여유 있는 집단에 편중될 수 있다는 건강 형평성 문제를 제기합니다. 또한 검사의 민감도 자체가 암 종류에 따라 크게 다르기 때문에, 어떤 암에 대해서는 탐지 능력이 매우 제한적일 수 있습니다.
Wade 등의 체계적 고찰은 현재까지 수집된 연구들이 대부분 환자-대조군 설계 또는 단일 코호트 연구임을 지적합니다[5]. 즉, 무증상 일반 인구를 대상으로 MCED 스크리닝이 실제로 생존율을 향상시키는지를 보여주는 고수준 근거가 아직 부족하다는 것입니다. Galleri와 CancerSEEK 모두 FDA 혁신 의료기기 지정(Breakthrough Device Designation)을 받았지만[3], 이는 승인이나 보험 급여 권고와는 다른 단계임을 구분할 필요가 있습니다.
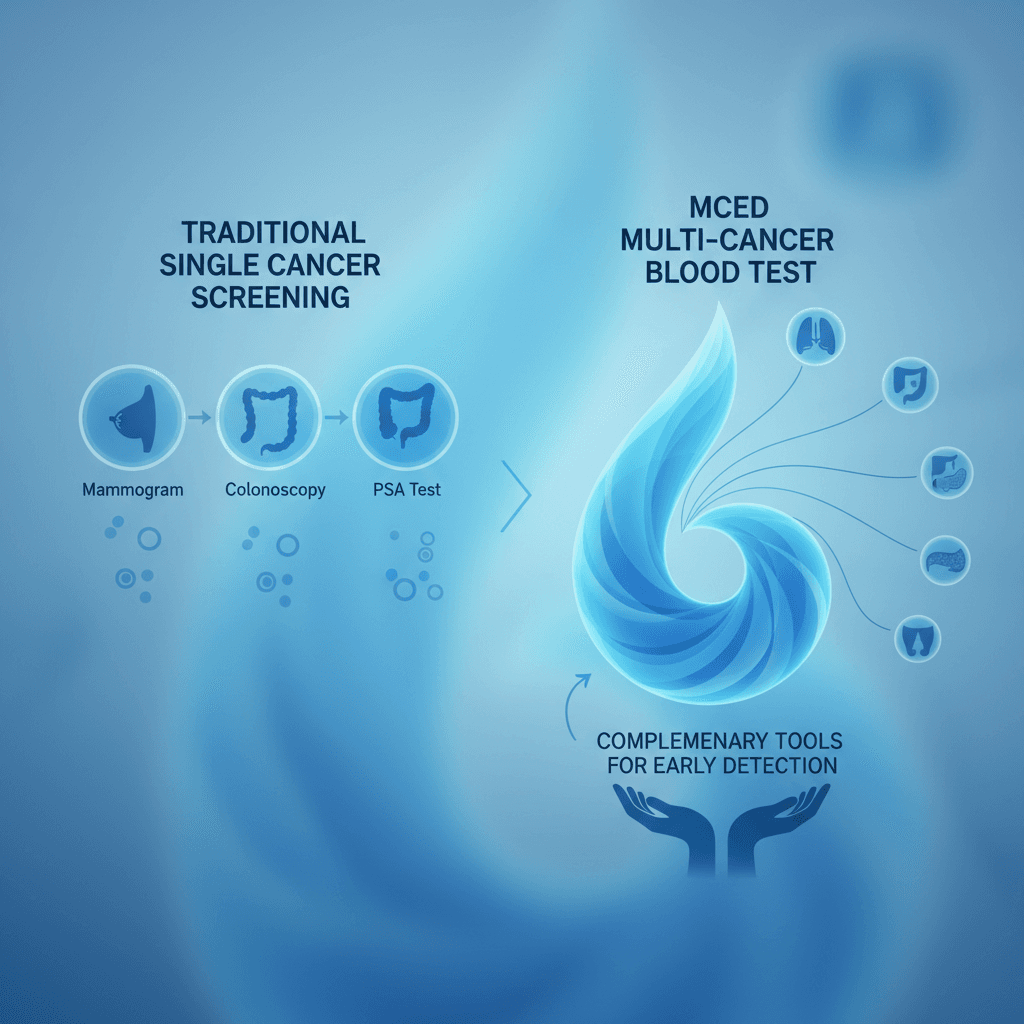
현재 의학계의 공통된 입장은 MCED 혈액검사가 기존의 단일 암 스크리닝을 대체하는 것이 아니라 보완하는 도구라는 점입니다. 대장내시경, 유방촬영술, 자궁경부세포검사 등 이미 임상적 유익성이 증명된 기존 검진 프로그램은 계속 이행하면서, MCED는 기존 스크리닝의 사각지대에 있는 암 종을 탐색하는 보조적 역할로 위치가 설정되고 있습니다.
PATHFINDER 연구에서 MCED를 통해 새로 진단된 암의 74%는 기존 권장 스크리닝의 해당 암 종이 아닌 암이었습니다[2]. 이 수치는 MCED가 현재의 표준 스크리닝으로는 발견하기 어려운 암 종을 잡아낼 수 있다는 가능성을 보여줍니다. 다만 이 연구에서 새로 진단된 29건 중 Stage I~II의 비율은 48%였으며, 나머지 절반은 진행성 병기에서 발견되었다는 점은 조기 발견의 효과가 제한적임을 시사합니다.
현재 임상 현장에서 가장 중요한 과제는 대규모 RCT 결과를 기다리는 일입니다. 영국에서는 NHS Galleri 시험이 140,000명 이상을 대상으로 진행 중이며, 미국에서도 여러 대형 연구가 진행되고 있습니다. 이 연구들이 사망률 감소 또는 치료 결과 개선을 증명한다면, 스크리닝 패러다임이 크게 바뀔 수 있습니다. 반대로, 기대에 미치지 못하는 결과가 나온다면 접근 방식의 전면 재검토가 필요할 것입니다.
암 조기발견의 전략에 관심 있는 경우에는 기존 암 조기발견 검사에 대한 종합 해설도 함께 살펴볼 수 있습니다. 기술의 발전과 함께 스크리닝의 기준이 어떻게 변화하고 있는지 맥락을 이해하는 데 도움이 됩니다. 결국, MCED가 임상 표준으로 자리 잡으려면 기술 성능의 향상과 함께 비용 접근성, 위양성 관리 체계, 그리고 장기 추적 근거가 함께 갖춰져야 한다는 것이 현재 전문가들의 공통된 시각입니다.
Q1. MCED 혈액검사는 현재 한국에서 받을 수 있습니까?
2026년 현재, MCED 검사는 주로 미국 임상 현장에서 활용되고 있으며 한국에서는 일반적인 건강검진 항목으로 제공되지 않습니다. Galleri, CancerSEEK 등의 제품은 미국에서 처방 기반으로 이용 가능하지만, 국내 급여 및 인허가 체계와는 별개이므로 국내 도입 여부는 관련 기관의 심사 결과에 따라 달라질 수 있습니다.
Q2. 특이도 99%라면 위양성이 거의 없는 것 아닙니까?
특이도 99%는 건강한 사람 100명 중 1명 정도에서 위양성이 나올 수 있다는 의미입니다. 그러나 수십만 명 규모의 대규모 스크리닝을 가정하면, 이 1%가 수천 명에 달할 수 있습니다. PATHFINDER 연구에서 양성 판정자 중 실제 암이 확인된 비율(PPV)은 43.1%였으므로, 절반 이상은 위양성이었습니다[2]. 특이도와 PPV는 다른 지표이며, 실제 임상 적용에서는 PPV가 더 직접적인 의미를 갖습니다.
Q3. 기존 암 스크리닝(대장내시경, 유방촬영술 등)과 병행해야 합니까?
현재 의학계 권고에 따르면, MCED 검사는 기존 스크리닝을 대체하지 않고 보완하는 도구로 사용하는 것이 적절합니다. 기존의 표준 검진 프로그램은 이미 임상적 유익성이 증명된 반면, MCED는 사망률 감소 효과를 입증할 대규모 RCT 결과가 아직 나오지 않은 상태입니다[4][5]. 기존 검진과 병행하되, 검사 결과의 해석은 반드시 의료진과 함께 해야 합니다.
Q4. 양성 결과가 나오면 어떻게 됩니까?
MCED 검사에서 암 신호 양성 결과가 나오면, 검사는 기원 조직(CSO) 정보를 함께 제공합니다. 이 정보를 바탕으로 의료진이 CT, PET, 내시경 등 추가 정밀 검사를 계획하게 됩니다. Marinac 등의 실세계 연구에서는 양성 판정 후 진단까지 걸린 시간의 중앙값이 39.5일이었습니다[7]. 양성 결과 자체가 곧 암 진단을 의미하는 것은 아니며, 반드시 후속 검사를 통한 확인이 필요합니다.
Q5. Stage I 민감도가 39%라면 조기 발견 효과가 있다고 볼 수 있습니까?
1기에서 민감도 39%는 조기 발견을 목적으로 하는 스크리닝 도구로서 아직 충분하지 않다는 평가가 일반적입니다[1][5]. 다만 현재 기존 스크리닝 프로그램이 존재하지 않는 암 종(예: 췌장암, 난소암)에 대해서는 낮은 민감도라도 기존 방법 대비 유의미한 추가 탐지 가능성을 가질 수 있습니다. 기술의 개선과 함께 민감도가 향상된다면 임상적 가치는 달라질 수 있으며, 이는 현재 진행 중인 대규모 연구들이 답해야 할 핵심 질문 중 하나입니다.
[1] Liu MC, et al. Sensitive and specific multi-cancer detection and localization using methylation signatures in cell-free DNA. Annals of Oncology. 2020. DOI: 10.1016/j.annonc.2020.02.011
[2] Schrag D, et al. Blood-based tests for multicancer early detection (PATHFINDER): a prospective cohort study. The Lancet. 2023. DOI: 10.1016/S0140-6736(23)01700-2
[3] Imai K, et al. Transforming cancer screening: the potential of multi-cancer early detection (MCED) technologies. International Journal of Clinical Oncology. 2025. DOI: 10.1007/s10147-025-02694-5
[4] Wan JCM, Sasieni P, Rosenfeld N. Promises and pitfalls of multi-cancer early detection using liquid biopsy tests. Nature Reviews Clinical Oncology. 2025. DOI: 10.1038/s41571-025-01033-x
[5] Wade R, et al. Multi-cancer early detection tests for general population screening: a systematic literature review. Health Technology Assessment. 2025. DOI: 10.3310/DLMT1294
[6] Walter CB, Groth C, von und zu Zwerger M. Evaluation of an innovative multi-cancer early detection test: high sensitivity and specificity in differentiating cancer, inflammatory conditions, and healthy individuals. Frontiers in Oncology. 2025. DOI: 10.3389/fonc.2025.1520869
[7] Marinac CR, et al. Real-world data and clinical experience from over 100,000 multi-cancer early detection tests. Nature Communications. 2025. DOI: 10.1038/s41467-025-64094-7
본 콘텐츠는 학술 논문과 공개된 연구 자료를 바탕으로 작성된 정보성 글이며, 의학적 진단이나 치료를 대체하지 않습니다. 건강 관련 결정은 반드시 담당 의료진과 상담하시기 바랍니다.