
대장 용종(colorectal polyp) 절제술을 받고 나면 '이제 다 끝난 것인가'라는 안도감과 함께 '언제 다시 검사해야 하는가'라는 불안감이 동시에 찾아오는 경우가 많습니다. 실제로 용종 제거 이후의 관리는 절제 자체만큼, 혹은 그보다 더 중요한 단계로 평가됩니다. 미국·유럽·영국의 주요 소화기 학회들이 공통적으로 권고하는 사후 관리 지침을 근거 중심으로 정리합니다.
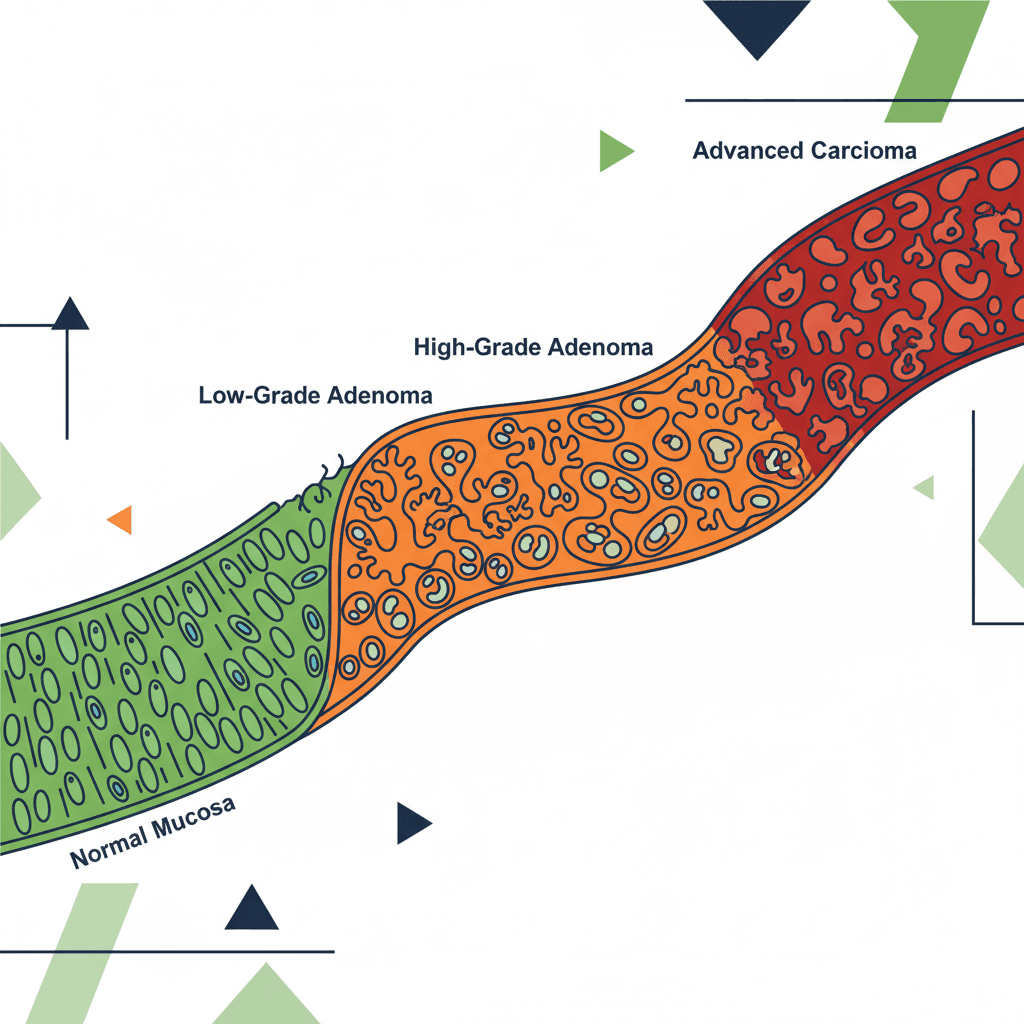
대장 용종, 특히 선종(adenoma)은 대장암(colorectal cancer, CRC)의 전구 병변으로 알려져 있습니다. 정상 점막 세포가 유전적·환경적 요인에 의해 이형성(dysplasia) 변화를 거쳐 선종이 되고, 다시 침습성 암으로 진행하는 이 일련의 경로를 선종-암 연속체(adenoma-carcinoma sequence)라고 부릅니다. 내시경으로 선종을 제거하면 이 연속체를 중간에 차단할 수 있다는 것이 폴립절제술(polypectomy)의 핵심 원리입니다.
2012년 《New England Journal of Medicine》에 발표된 Zauber 등의 장기 코호트 연구는 이 원리를 수치로 뒷받침합니다. 선종성 용종을 내시경으로 제거한 집단을 평균 15.8년간 추적한 결과, 대장암으로 인한 사망률이 절제를 받지 않은 일반 집단 대비 53% 낮게 나타났습니다(표준화 사망비 SMR = 0.47, 95% CI 0.26~0.80)[1]. 단순한 이론적 예방 효과가 아니라 실질적인 사망률 감소를 장기 데이터로 확인한 연구라는 점에서 높이 평가됩니다.
그러나 절제 이후에도 새로운 선종이 생길 수 있습니다. 이것이 사후 감시(surveillance) 내시경이 필요한 이유입니다. 2014년 노르웨이 레지스트리 기반 코호트 연구(n=40,826)에서는 저위험 선종 절제 환자의 경우 사망률이 일반 인구보다 낮았지만(SMR 0.75), 고위험 선종 절제 환자에서는 오히려 약간 높은 사망률(SMR 1.16)이 관찰되었습니다[2]. 고위험군은 절제만으로 위험이 해소되지 않으며, 지속적인 추적 관찰이 필수적이라는 사실을 보여주는 데이터입니다.
절제 후 재발 위험은 최초 용종의 크기, 개수, 조직 유형, 이형성 등급에 따라 크게 달라집니다. 이 변수들을 바탕으로 환자를 위험도 그룹으로 나누고, 그에 맞는 재검 주기를 설정하는 것이 현대 임상 지침의 핵심 방향입니다. 직접적인 절제 효과와 장기 추적 관리는 서로 분리할 수 없는 한 쌍의 의료 행위로 이해하는 것이 적절합니다.
용종 절제 후 다음 내시경 검사 시기는 처음 발견된 용종의 특성에 따라 결정됩니다. 미국 다학회 대장암 태스크포스(US Multi-Society Task Force on Colorectal Cancer, USMSTF)의 2020년 합의 업데이트는 가장 광범위하게 인용되는 기준 중 하나입니다[3].
USMSTF 기준에 따르면, 1~2개의 소형(직경 <10mm) 관상 선종(tubular adenoma)은 저위험군으로 분류되어 7~10년 후 재검이 권고됩니다. 반면 직경 10mm 이상의 선종, 융모성 조직(villous histology), 고등급 이형성(high-grade dysplasia, HGD), 또는 10mm 미만 선종이 3개 이상인 경우 고위험군으로 분류되어 3년 후 재검이 권고됩니다. 고위험군의 누적 고등급 선종 발생률은 16~19%로 추산됩니다.
유럽 소화기내시경학회(European Society of Gastrointestinal Endoscopy, ESGE)의 2020년 업데이트 가이드라인은 일부 기준이 다릅니다[4]. ESGE는 저등급 이형성을 동반한 소형 선종(<10mm)에 대해 추가 감시가 불필요하며, 10년 후 표준 검진으로 복귀하면 충분하다는 입장입니다. 그러나 직경 10mm 이상, 고등급 이형성, 선종 5개 이상, 또는 직경 10mm 이상의 톱니모양 용종(serrated polyp)의 경우에는 3년 감시를 권고합니다. 또한 직경 20mm 이상의 병변을 분할 절제(piecemeal resection)한 경우에는 절제 후 3~6개월 내 조기 추적 내시경이 필요합니다.
영국 소화기학회(British Society of Gastroenterology, BSG)의 가이드라인도 3년 감시 기준에서는 큰 이견이 없습니다[5]. 고위험 기준은 2개 이상의 용종 중 1개 이상이 고등급 병변이거나, 전암성 용종이 5개 이상인 경우입니다. 이 경우 단 한 차례의 감시 내시경을 3년 후 시행합니다. 네 가이드라인을 비교한 2021년 리뷰는 저위험군 처리 방식에서 차이가 있지만, 고위험군에 대한 3년 감시 권고는 모든 가이드라인에서 일치한다고 정리했습니다[6].
실제 임상 현장에서는 이러한 분류가 의사의 판단과 결합하여 적용됩니다. 예를 들어 50대 초반의 A씨는 1cm 관상 선종 1개를 절제한 후 3년 재검 권고를 받았는데, 이는 크기 기준(10mm)에 해당하는 고위험 경계에 위치하기 때문이었습니다. 40대 중반의 B씨는 6mm 선종 1개만 발견되어 절제 후 10년 표준 검진 일정을 유지하고 있습니다. 같은 '용종 제거'라도 재검 주기가 크게 달라질 수 있는 이유가 여기에 있습니다.
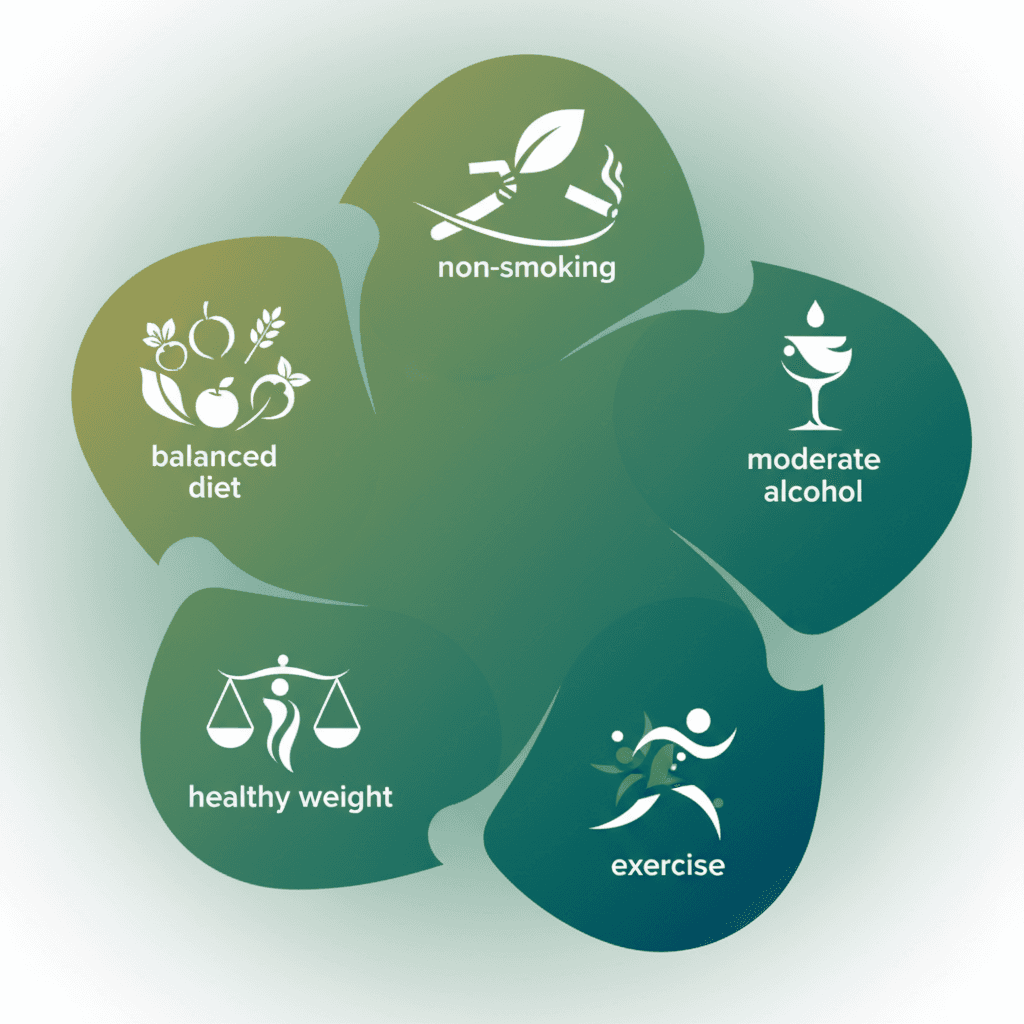
용종 절제 이후의 생활습관은 새로운 선종 발생과 대장암 위험에 실질적인 영향을 미칩니다. 2022년 《International Journal of Cancer》에 발표된 전향적 코호트 연구(n=24,668)는 내시경 절제술 이후 환자들을 대상으로 건강한 생활습관 요인의 수와 대장암 발생률 및 전체 사망률 사이의 관계를 분석했습니다[7]. 이 연구에서 건강한 생활습관 요인으로 정의된 항목은 비흡연, 절주, 규칙적 신체 활동, 건강 체중 유지, 건강한 식단 등 다섯 가지였습니다.
분석 결과, 이 다섯 가지 요인 중 4~5개를 충족하는 그룹은 0~1개를 충족하는 그룹에 비해 대장암 발생 위험이 약 48% 낮았습니다(상대위험도 RR ~0.52). 전체 사망률도 44% 낮게 나타났습니다(RR ~0.56). 수술 또는 내시경 절제 이후의 생활습관 변화가 장기 예후에 통계적으로 유의미한 영향을 미친다는 것을 보여주는 대규모 근거입니다.
식단과 관련해서는 적색육(red meat) 및 가공육 섭취 감소, 식이섬유 섭취 증가, 과일·채소 중심의 식단이 대장암 1차 예방 근거와 유사한 방향으로 권고됩니다. 알코올은 대장암의 독립적 위험 인자로 알려져 있으며, 절제 이후에도 섭취량을 최소화하는 것이 임상 가이드라인의 일반적인 방향입니다. 신체 활동은 인슐린 저항성과 전신 염증 지표를 낮추는 기전을 통해 선종 재발 위험을 줄이는 것으로 해석됩니다.
비만, 특히 내장지방 축적은 대장 점막의 만성 염증 환경과 관련이 있으며, 이는 선종 재발의 촉진 요인으로 작용할 수 있습니다. 체질량지수(body mass index, BMI) 조절과 복부 비만 감소는 절제 후 관리에서 중요한 비약물 요소로 자리잡고 있습니다. 담당 의사와 정기적인 상담을 통해 개인별 목표를 설정하고 생활습관 전반을 점검하는 것이 장기적인 재발 예방의 기반이 됩니다. 대장암 예방과 관련된 식단 원칙에 대해서는 대장암 예방 식단 가이드에서 추가로 확인할 수 있습니다.
약물을 통한 화학적 예방(chemoprevention) 가능성도 연구가 축적되어 있습니다. 가장 많이 연구된 물질은 아스피린(aspirin)입니다. 2009년 《Colorectal Disease》에 발표된 무작위 대조 시험(RCT) 메타분석(n=2,175)은 아스피린이 대장 선종 재발에 미치는 영향을 분석했습니다[8]. 전체 선종 재발에서 상대위험도(relative risk, RR)는 0.836으로 감소 경향이 나타났으며, 고등급 선종 재발에서는 RR 0.655로 약 35%의 감소 효과가 관찰되었습니다.
아스피린의 작용 기전으로는 시클로옥시게나제-2(COX-2) 억제를 통한 프로스타글란딘(prostaglandin) 생성 감소와 대장 점막 내 염증 경로 차단이 제시됩니다. 이 기전은 선종 형성의 초기 단계, 즉 염증성 미세환경을 억제하는 방향으로 작동하는 것으로 알려져 있습니다. 단, 위장관 출혈과 같은 부작용 위험이 존재하기 때문에 아스피린의 예방적 사용은 개인의 출혈 위험, 기저 질환, 기존 복용 약물을 종합적으로 평가한 의사의 판단 하에 결정되는 사항입니다.
현재 미국 암 학회 및 USMSTF를 포함한 주요 기관들은 아스피린을 모든 용종 절제 환자에게 일률적으로 사용하도록 권고하지 않습니다. 심혈관 질환 예방을 위해 이미 저용량 아스피린을 복용 중인 환자라면 대장 선종 예방에 부가적인 효과를 기대할 수 있다는 것이 현재의 임상적 이해입니다. 이 분야는 현재도 연구가 진행 중이며, 향후 지침이 업데이트될 가능성이 있습니다.
이와 별도로, 칼슘 보충제와 비타민 D가 선종 재발 예방에 효과가 있는지에 대한 연구도 지속되고 있습니다. 현재까지의 근거는 일관적이지 않으며, 일부 연구에서 긍정적 신호가 나타났지만 모든 가이드라인에서 권고하는 수준의 근거는 아직 부족합니다. 화학적 예방 전략은 생활습관 개선을 보완하는 역할로서, 단독으로 의존하기보다는 정기적인 감시 내시경과 함께 통합적 관리 체계 안에서 논의되어야 합니다.

Q1. 용종을 제거했는데 왜 또 내시경을 받아야 하는가?
용종 절제는 기존 병변을 제거하는 것이며, 새로운 선종이 이후에 발생할 가능성은 여전히 존재합니다. 특히 고위험군으로 분류된 경우에는 처음 절제 후에도 16~19%의 누적 고등급 선종 발생률이 보고되어 있습니다[3]. 감시 내시경은 새로 생긴 병변을 조기에 발견하고 제거하기 위한 예방 절차입니다.
Q2. 저위험 선종이라고 들었는데 재검을 받지 않아도 되는가?
유럽(ESGE) 및 영국(BSG) 가이드라인에 따르면, 저등급 이형성을 동반한 소형 선종(<10mm)은 추가 감시 없이 10년 표준 검진으로 복귀하는 것이 권고됩니다[4,5]. 그러나 미국(USMSTF) 기준에서는 동일 상황에서도 7~10년 후 추적 내시경을 권고합니다[3]. 담당 의사가 적용하는 지침과 개인적 위험 요인에 따라 달라질 수 있으므로 진료 시 직접 확인하는 것이 중요합니다.
Q3. 용종 절제 후 식단은 어떻게 바꾸어야 하는가?
특정 음식을 완전히 금지하는 획일적 기준은 없습니다. 다만 임상 연구에서는 적색육·가공육 감소, 식이섬유 증가, 알코올 최소화, 과일·채소 중심의 식단이 대장암 위험 감소와 관련이 있는 것으로 나타났습니다. 건강한 생활습관 요인을 4~5개 갖춘 경우 대장암 재발 위험이 약 48% 낮다는 전향적 연구 결과가 있습니다[7].
Q4. 아스피린이 용종 재발을 예방한다고 들었는데, 직접 복용해도 되는가?
아스피린이 고등급 선종 재발을 약 35% 줄인다는 메타분석 결과가 있습니다[8]. 그러나 위장관 출혈 등의 부작용 위험이 존재하며, 모든 절제 후 환자에게 일률적으로 권고되지는 않습니다. 복용 여부는 개인의 출혈 위험, 심혈관 병력, 현재 복용 약물 등을 고려하여 담당 의사와 상의 후 결정하는 사항입니다.
Q5. 분할 절제(piecemeal resection)를 받았는데 3~6개월 후 내시경이 필요한 이유는 무엇인가?
직경 20mm 이상의 큰 병변을 한 번에 완전히 제거하지 못하고 여러 조각으로 나누어 절제한 경우, 잔존 조직이 남아 있을 가능성이 있습니다. ESGE 가이드라인은 이 경우 절제 후 3~6개월 내에 조기 추적 내시경을 시행하여 잔존 병변 여부를 확인하도록 권고합니다[4]. 조기 확인을 통해 불완전 절제의 위험을 최소화하는 것이 목적입니다.
Zauber AG, Winawer SJ, O'Brien MJ, et al. Colonoscopic polypectomy and long-term prevention of colorectal-cancer deaths. N Engl J Med. 2012;366(8):687-696. doi:10.1056/NEJMoa1100370
Løberg M, Kalager M, Holme O, et al. Long-term colorectal-cancer mortality after adenoma removal. N Engl J Med. 2014;371(9):799-807. doi:10.1056/NEJMoa1315870
Gupta S, Lieberman D, Anderson JC, et al. Recommendations for follow-up after colonoscopy and polypectomy: A consensus update by the US Multi-Society Task Force on Colorectal Cancer. Gastroenterology. 2020;158(4):1131-1153. doi:10.1053/j.gastro.2019.10.026
Hassan C, Antonelli G, Dumonceau JM, et al. Post-polypectomy colonoscopy surveillance: European Society of Gastrointestinal Endoscopy (ESGE) guideline — update 2020. Endoscopy. 2020;52(8):687-700. doi:10.1055/a-1185-3109
Rutter MD, East J, Rees CJ, et al. British Society of Gastroenterology/Association of Coloproctology of Great Britain and Ireland/Public Health England post-polypectomy and post-colorectal cancer resection surveillance guidelines. Gut. 2020;69(2):201-223. doi:10.1136/gutjnl-2019-319858
Abu-Freha N, Abufreha R, Abu-Rass H, et al. Post-polypectomy surveillance colonoscopy: Comparison of the updated guidelines. United European Gastroenterol J. 2021;9(7):745-752. doi:10.1002/ueg2.12106
Wang L, Lo CH, He X, et al. Adherence to a healthy lifestyle in relation to colorectal cancer incidence and all-cause mortality after endoscopic polypectomy. Int J Cancer. 2022;151(8):1224-1233. doi:10.1002/ijc.34176
Gao F, Liao C, Liu L, et al. The effect of aspirin in the recurrence of colorectal adenomas: a meta-analysis of randomized controlled trials. Colorectal Dis. 2009;11(9):893-901. doi:10.1111/j.1463-1318.2008.01746.x
본 콘텐츠는 학술 논문과 공개된 연구 자료를 바탕으로 작성된 정보성 글이며, 의학적 진단이나 치료를 대체하지 않습니다. 건강 관련 결정은 반드시 담당 의료진과 상담하시기 바랍니다.